Endlich volljährig! – Die HPV-Impfung wird 18!
Endlich volljährig! – Die HPV-Impfung wird 18!
Der erste Impfstoff gegen Humane Papillomviren (HPV) ist vor 18 Jahren – im September 2006 – auf den Markt gekommen. Was ist seitdem passiert? Welchen Herausforderungen müssen wir uns heute stellen?

Eine Infektion mit humanen Papillomviren (HPV) kann neben Genitalwarzen bestimmte Krebsarten verursachen, wie beispielsweise Gebärmutterhalskrebs und Analkarzinome.1 Die wichtigste Präventionsmaßnahme gegen bestimmte HPV-assoziierte Erkrankungen stellt die HPV-Impfung dar.2 Im September 2006 – vor 18 Jahren – kam mit Gardasil® der erste HPV-Impfstoff in Europa auf den Markt.3, 4 Zeit für einen Rückblick darauf, wie die HPV-Impfung erwachsen geworden ist!
Warum gegen HPV impfen?
Infektionen mit HPV zählen zu den häufigsten sexuell übertragbaren Infektionen.2 Sie sind sowohl bei der Frau als auch beim Mann weltweit sehr verbreitet und können während des gesamten Lebens erfolgen.2, 5 So infizieren sich die meisten sexuell aktiven Menschen mindestens einmal im Leben mit HPV.2
In Deutschland erkranken jährlich etwa 6.250 Frauen und ca. 1.600 Männer an HPV-bedingten Karzinomen.2 Der häufigste HPV-induzierte Tumor ist das Zervixkarzinom, an dem in Deutschland 2019 rund 1.600 Betroffene starben.2, 6 Laut einer Studie, die 2017 veröffentlicht wurde, zur Krankheitslast durch Krebs, präkanzeröse Läsionen und Genitalwarzen, die auf bestimmte HPV-Impfstofftypen zurückzuführen sind, waren HPV-Infektionen bei Männern und Frauen in Europa für einen nennenswerten Anteil von bestimmten Krebserkrankungen u. a. an Vulva, Vagina, Anus und nicht zuletzt Genitalwarzen verantwortlich (Abb. 1).7
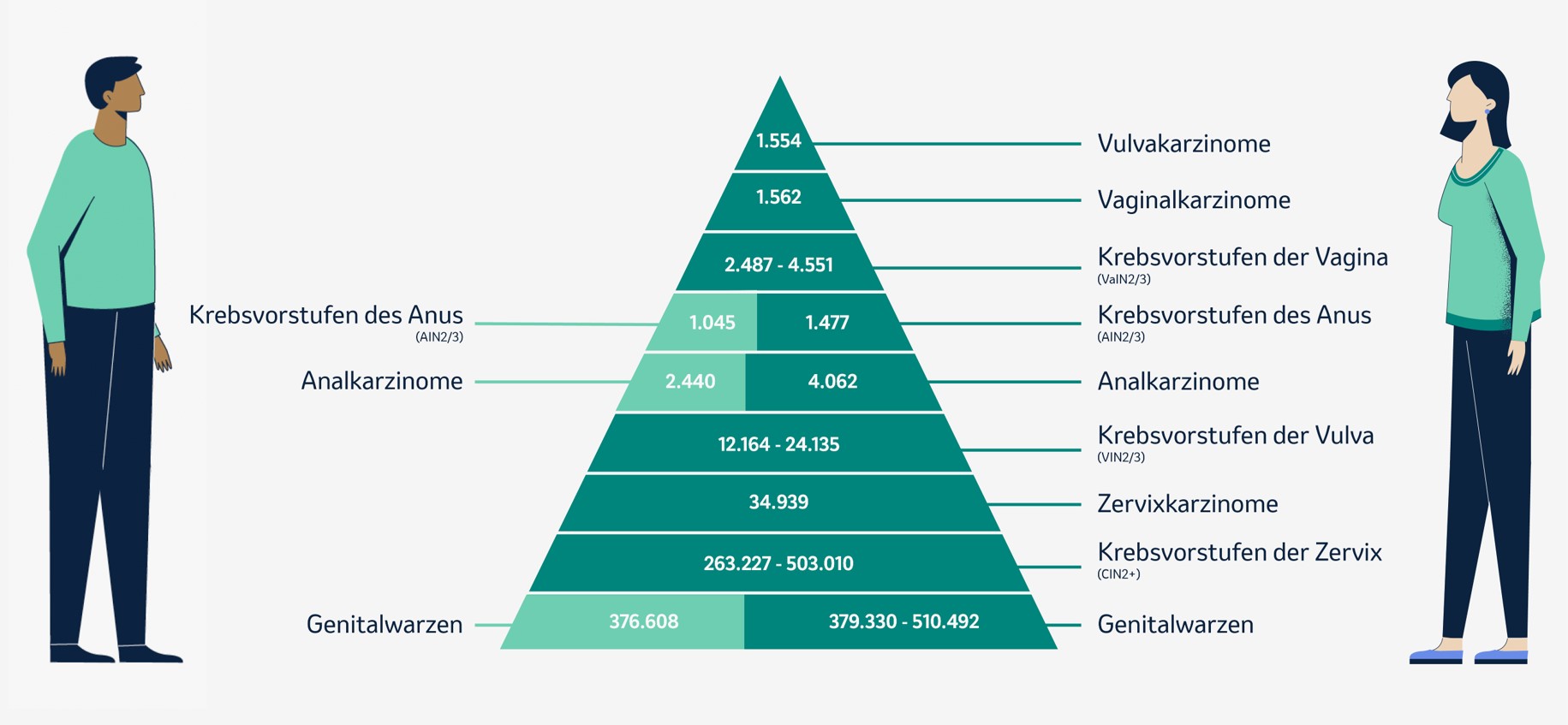
Abbildung 1: Auszug aus den geschätzten jährlichen Neuerkrankungen an HPV-assoziierten Neoplasien bei Frauen und Männern in Europa. Schätzung der Inzidenzen basierend auf der Datenbank der IARC (International Agency for Research on Cancer), den Eurostat Population Data sowie weiterer Literatur (mod. von MSD nach Hartwig S et al. 2017)#.
HPV-Impfung als wichtigste Präventionsmaßnahme
Die wichtigste Präventionsmaßnahme, um bestimmten HPV-assoziierten Erkrankungen vorbeugen zu können, ist die HPV-Impfung.2 Zur Reduktion der Krankheitslast durch bestimmte HPV-assoziierte Tumoren empfiehlt die STIKO eine frühzeitige Impfung im Alter von 9–14 Jahren.8 Versäumte Impfungen sollen bis zum Tag vor dem 18. Geburtstag nachgeholt werden, z. B. mit GARDASIL® 9.8, 9
HPV-Impfung mit GARDASIL® 9
GARDASIL® 9 ist ab einem Alter von 9 Jahren ohne Altersobergrenze gegen folgende HPV-Erkrankungen indiziert:9
- Vorstufen maligner Läsionen und Karzinome, die die Zervix, Vulva, Vagina und den Anus betreffen und die durch die Impfstoff-HPV-Typen verursacht werden.
- Genitalwarzen (Condylomata acuminata), die durch spezifische HPV-Typen verursacht werden.
Belastung und indirekte Kosten der durch Impfungen vermeidbaren Krebssterblichkeit in Europa
Eine im Jahr 2024 veröffentlichte Studie nutzte ein Modell, das die wirtschaftliche Belastung für die Gesellschaft widerspiegelte, indem es den Produktivitätsverlust* aufgrund der vorzeitigen Sterblichkeit durch potenziell vermeidbare Krebserkrankungen schätzte.10 Dazu gehörten neben Hepatis B-bedingten Krebsarten auch HPV-assoziierte Krebserkrankungen in 40 europäischen Ländern, darunter Deutschland.10 Insgesamt führten im Jahr 2019 31.906 HBV- und HPV-bedingte Krebstodesfälle zu einem Produktivitätsverlust von 18,5 Milliarden Euro in Europa.10 HPV-assoziierter Gebärmutterhalskrebs hatte die höchste Sterblichkeit mit 19.473 Todesfällen und die höchste wirtschaftliche Belastung mit 10,7 Milliarden Euro.10 Deutschland gehörte in Bezug auf HBV- und HPV-bedingte Todesfälle zu den Ländern mit der höchsten Sterblichkeit (n = 4.605), gefolgt von Frankreich (n = 3.348) und der Ukraine (n = 3.051).10 Zudem wies Deutschland den höchsten Produktivitätsverlust* mit 3.733.134.848 Euro auf.10
Die Daten unterstreichen die hohe Sterblichkeit und Produktivitätsverluste in Europa aufgrund von HPV- und HBV-bedingten Krebserkrankungen, die durch Maßnahmen der öffentlichen Gesundheit wie Screening und Impfung reduziert werden könnten.10
HPV-Impfung – das Erwachsenwerden
Die HPV-Impfung stellt die wichtigste Präventionsmaßnahme dar, um bestimmten HPV-assoziierten Erkrankungen vorbeugen zu können.2 In Deutschland sind derzeit zwei verschiedene HPV-Impfstoffe verfügbar:11 Cervarix® und Gardasil® 9.12, 13 Doch wie fing alles an? Werfen wir einen Blick auf die Chronologie der HPV-Impfstoffentwicklung:
Ihre Forschungsursprünge hat die HPV-Impfung in Deutschland.14 Seit den 1970er-Jahren forschte der deutsche Mediziner Prof. Harald zur Hausen zu dem Zusammenhang zwischen HP-Viren und der Entstehung von Zervixkarzinomen.14, 15 Seine Forschungsarbeiten führten noch in den 1990er-Jahren zu den ersten klinischen Impfstoffstudien.16 Die klinische Forschung mündete 2006 in der Zulassung von Gardasil® (Abbildung 2).3 Der tetravalente Impfstoff richtete sich gegen die HPV-Typen 16 und 18 sowie 6 und 11 und fand zunächst zur Prävention von Vorstufen maligner Läsionen im Genitalbereich (Zervix, Vulva) und Zervixkarzinomen sowie Genitalwarzen Anwendung.3 2010 erhielt dieser Impfstoff eine Zulassungserweiterung, die ebenfalls maligne Läsionen der Vagina einschloss.17 2014 wurde die Zulassung um maligne Läsionen im Analbereich und Analkarzinome erweitert.18 Aufgrund der Einführung eines neuen, nonavalenten Impfstoffs ist der tetravalente Impfstoff in Deutschland nicht mehr verfügbar.19 2007 erhielt ein weiterer HPV-Impfstoff die Zulassung in Europa. Der bivalente Impfstoff kann ebenfalls vor den Hochrisiko-HPV-Typen 16 und 18 schützen.20 Entsprechend dieser HPV-Typen war der Impfstoff zur Prävention von prämalignen genitalen Läsionen der Zervix und Zervixkarzinomen und ab 2013 auch von prämalignen genitalen Läsionen der Vulva und Vagina indiziert.20, 21 Ähnlich wie beim tetravalenten Impfstoff wurde anschließend im Jahr 2016 das Anwendungsgebiet um Läsionen des Anus und Analkarzinome erweitert.22
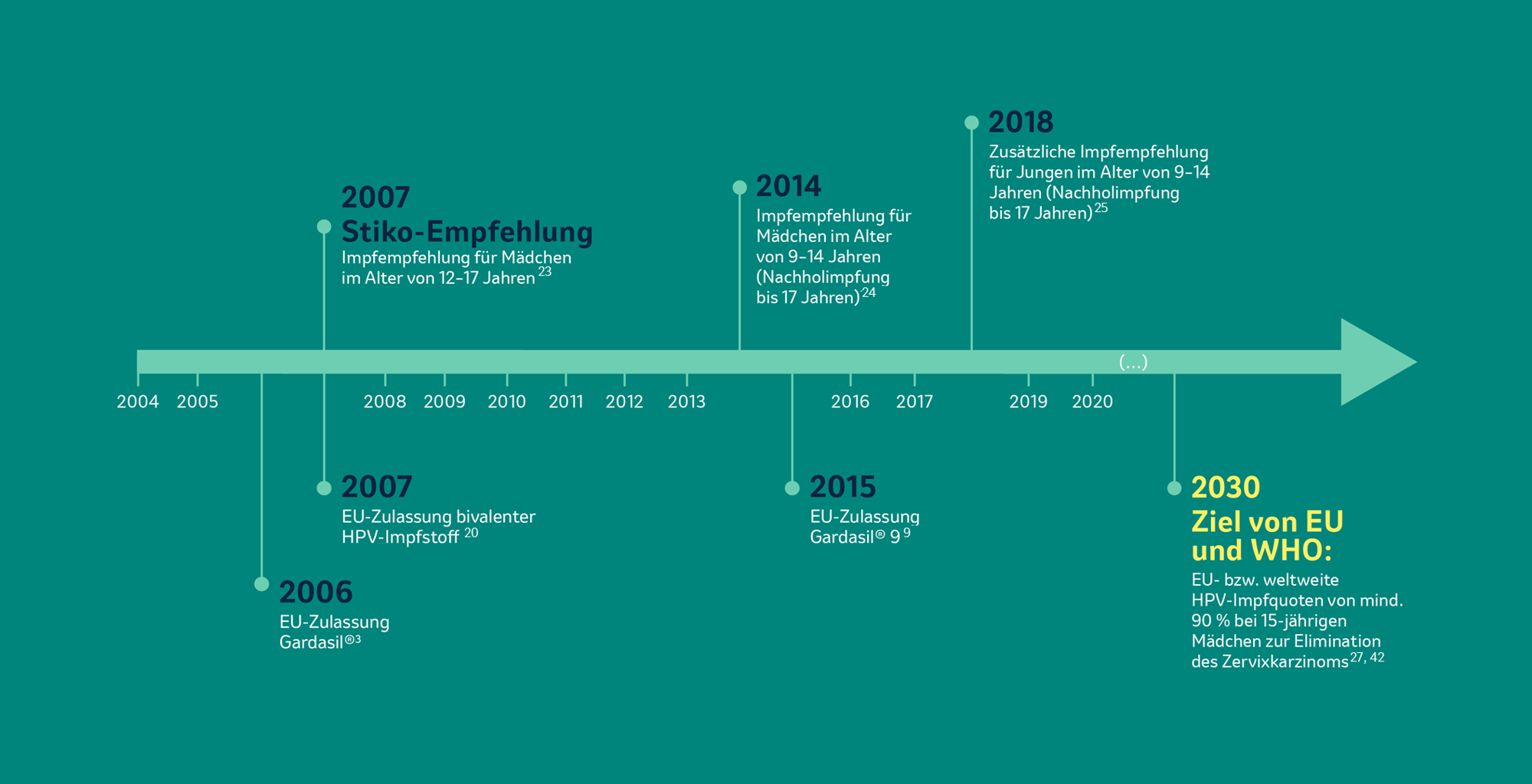
Abbildung 2: Entwicklung der HPV-Impfstoffe und der STIKO-Empfehlung zur HPV-Impfung in Deutschland sowie die Ziele von EU und WHO in Bezug auf HPV-Impfquoten auf einem Zeitstrahl. Abbildung erstellt von MSD.3, 20, 23, 24, 13, 25–27
Seit 2015 gibt es mit Gardasil® 9 einen nonavalenten Impfstoff auf dem deutschen Markt, der im Vergleich zu Gardasil® gegen fünf weitere Hochrisiko-HPV-Typen schützen kann: 31, 33, 45, 52 und 58. Basierend auf epidemiologischen Studien nimmt man an, dass Gardasil® 9 so vor den HPV-Typen schützen kann, die für u. a. etwa 90 % der Zervixkarzinome verantwortlich sind.9 Weltweit konnten bereits über 734 Millionen HPV-Impfstoffdosen von Gardasil® und Gardasil® 9 ausgeliefert werden.28
Die STIKO-Impfempfehlungen im Wandel der Zeit
Seit 2007 empfiehlt die Ständige Impfkommission (STIKO) die HPV-Schutzimpfung für Mädchen – zuerst im Alter von 12–17 Jahren (Abbildung 2).23 2014 wurde die Impfempfehlung angepasst und das Alter auf 9–14 Jahre herabgesetzt mit Nachholimpfung bis 17 Jahre.24 Seit 2018 schließt diese Empfehlung auch Jungen im Alter von 9–14 Jahren ein.25 Sowohl bei Jungen als auch bei Mädchen sollen spätestens bis zum Alter von 17 Jahren versäumte Impfungen gegen HPV nachgeholt werden.8
Nicht nur die Impfung ist volljährig, auch volljährige Personen können sich gegen HPV impfen lassen, denn wie die STIKO bestätigt, können junge Erwachsene auch nach dem Erreichen des 18. Lebensjahrs noch individuell von einer Impfung profitieren – auch wenn sie bereits infiziert sind.11 Denn persistierende HPV-Infektionen sind eher Einzelinfektionen, sodass eine Impfung gegebenenfalls Schutz vor den anderen im Impfstoff enthaltenen HPV-Typen bieten kann, mit denen man noch nicht infiziert ist.11 Die Wirksamkeit bzw. Immunogenität von GARDASIL® 9 (beruhend auf dem Nachweis der Wirksamkeit des 4v-HPV-Impfstoffs) wurde zudem auch bei Erwachsenen bis 45 Jahren in Studien untersucht.9
Aufgrund der aktuellen STIKO-Empfehlung sind Krankenkassen nur verpflichtet, die HPV-Impfung für Jugendliche im Alter von 9–14, bzw. Nachholimpfungen bis zum 18. Geburtstag zu übernehmen.8, 29 Viele gesetzliche Krankenkassen haben ihre Leistungen jedoch darüber hinaus freiwillig ausgeweitet und erstatten bei Bedarf die HPV-Impfung für Patienten zwischen 18 und 26 Jahren.30, 31 Auf Nachfrage werden aber auch häufig die Kosten für Patienten über einem Alter von 26 Jahren erstattet.32
Finden Sie hier noch mehr Informationen zur HPV-Impfung über 18.
Benötigen Sie noch weitere Informationen zur Abrechnung der HPV-Impfung bei jungen Erwachsenen? In diesem Beitrag haben wir für Sie Tipps zur Abrechnung der HPV-Impfung zusammengestellt.
Bisher Erreichtes
Die HPV-Impfung stellt die wichtigste Präventionsmaßnahme dar, um bestimmten HPV-assoziierten Erkrankungen vorbeugen zu können.2 In verschiedenen Studien zeigte sich, dass die Einführung der HPV-Impfung zu einer Reduktion des Zervixkarzinomrisikos führen konnte.33, 34 Studiendaten aus Bayern zeigten ein um 63 % (aHR 0,37 (95 %-KI: 0,34–0,40) reduziertes Risiko für HPV-bedingte Genitalwarzen bei vollständig gegen HPV geimpften Frauen im Vergleich zu Ungeimpften.35
Mehr zum Effekt der HPV-Impfung auf das Risiko, an einem Zervixkarzinom zu erkranken, finden Sie in diesem Artikel.
Aktuelle Daten zur Zervixkarzinom-Inzidenz in Deutschland
Daten zu neu diagnostizierten HPV-assoziierten Zervixkarzinomen von 2004 bis 2018 vom Zentrum für Krebsregisterdaten bildeten die Grundlage für eine deutsche Studie zur Schätzung von Inzidenztrends (invasiv und in situ).36 Dabei konnte gezeigt werden, dass der säkulare Anstieg der Inzidenz des Zervixkarzinoms seit 2010 rückläufig ist und in allen Altersgruppen der impfberechtigten Frauen deutlich abgenommen hat.36 Beispielsweise sank die Inzidenz in der Altersgruppe 24–26 Jahre von 70,0 auf 41,8 Fälle pro 100.000 Frauen im Zeitraum 2010–2018.36 Die Geburtskohorte von 1992, die als erste impfberechtigt war, zeigt eine um 24 % niedrigere Inzidenz als die Referenzkohorte von 1989 mit einem relativen Risiko von 0,76 (95 %-KI: 0,68–0,86).36 In späteren Geburtskohorten, mit zunehmender Impfquote, ist der Effekt noch größer.36
Es ist anzumerken, dass die dargestellten Trends der Inzidenzraten in dieser Modellierungsstudie auf einer Hochrechnung ausgewählter Landeskrebsregister auf Gesamtdeutschland beruhen.36 Diese Inzidenzraten wurden den HPV-Impfraten im zeitlichen Verlauf entgegengestellt.36 Die Daten lassen keinen direkten Rückschluss zwischen dem Impfstatus der Patientinnen und dem Zervixkarzinomrisiko zu, da keine patientenbezogenen Daten ausgewertet wurden.36 Dennoch lassen die Studienergebnisse erwarten, dass die Effekte der HPV-Impfung in den nächsten 5–10 Jahren noch deutlicher werden könnten, wenn die Impfkohorten in Altersgruppen mit höheren Inzidenzen eintreten.36 Weitere Untersuchungen zur Inzidenzentwicklung bei impfberechtigten Frauen sind allerdings erforderlich. Wechselbeziehungen mit dem 2020 eingeführten Zervixkarzinom-Screeningprogramm und der STIKO-Empfehlung für Jungen ab 2018 sollten dabei berücksichtigt werden.8, 36
HPV-Impfquoten in Deutschland
Trotz der verfügbaren Studiendaten, der Impfempfehlung durch die STIKO und der vollen Erstattung durch die Krankenkassen sind bislang nicht genug Jugendliche in Deutschland vollständig gegen HPV geimpft: Betrachtet man die HPV-Impfquoten von 15-jährigen Mädchen in Deutschland von 2011–2020, so lag die Impfquote für eine vollständige Impfserie im Jahr 2011 bundesweit bei 27,2 %, stieg in den Folgejahren ab 2014 leicht an auf über 30 %, bis im Jahr 2020 51 % erreicht wurden (Abb. 3). Vorläufige Ergebnisse zeigen, dass dieser Trend auch 2021 fortgesetzt wird.37
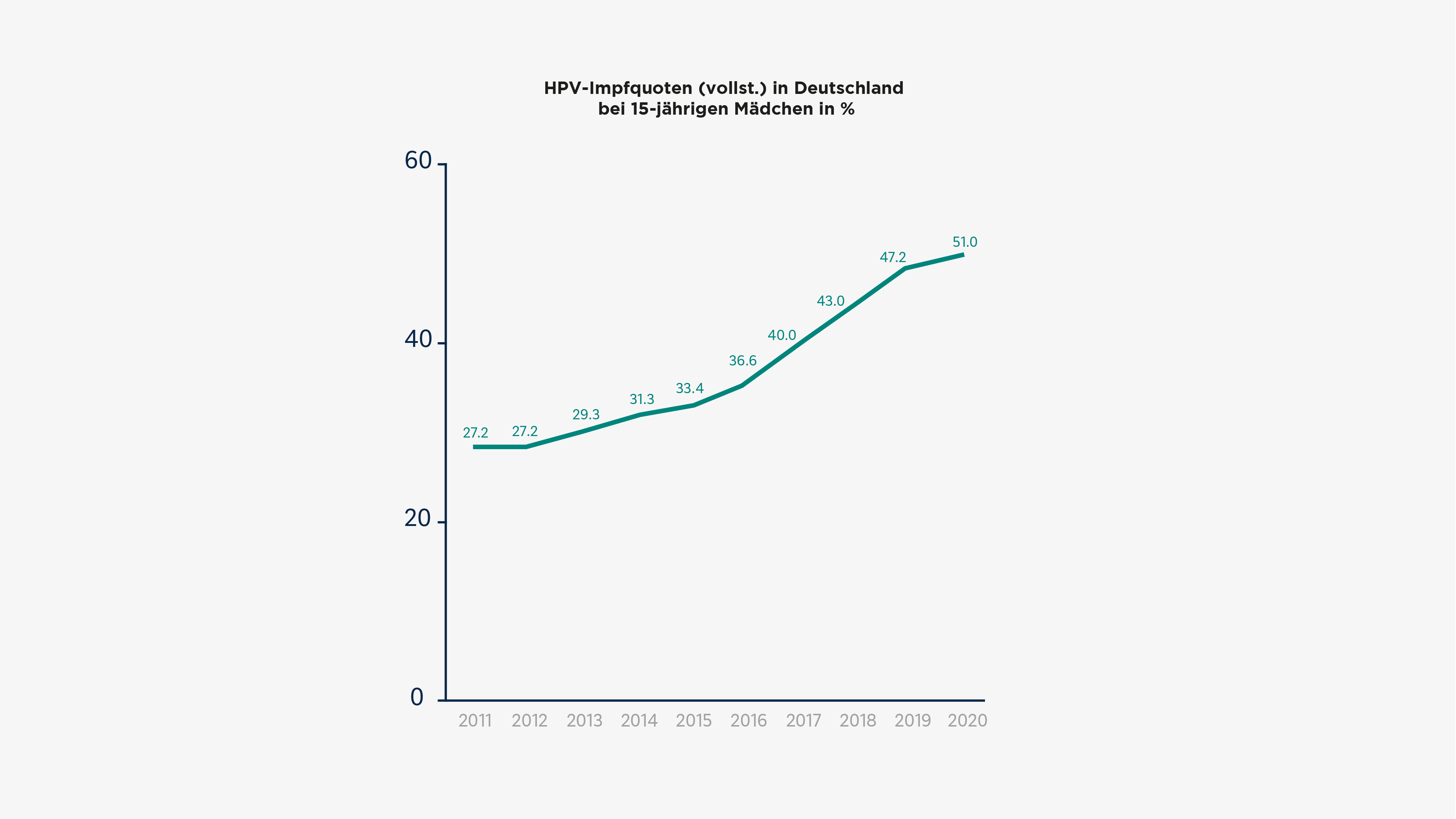
Abbildung 3: HPV-Impfquoten (vollständige Impfserie) von 15-jährigen Mädchen in Deutschland von 2011–2020. Abbildung modifiziert von MSD.37
Bei Mädchen im Alter von 18 Jahren waren die HPV-Impfquoten im Jahr 2020 für eine vollständige Impfserie im selben Jahr mit 54,1 % nur geringfügig höher. Bei den 18-jährigen Jungen war nicht einmal jeder Zehnte (8,1 %) vollständig geimpft.37
Wie aus einer aktuellen Studie hervorgeht, sind die HPV-Impfquoten bei Jungen in Deutschland in den sechs Jahren nach der Impfempfehlung allerdings gestiegen und dies trotz der Umstände der COVID-19-Pandemie: So hatten bis Ende 2021 geschätzt 44,4 % der 15-jährigen Jungen und 29,7 % der 18-jährigen Jungen eine erste Impfdosis erhalten.38
HPV-Impfungen: Wo steht Deutschland im internationalen Vergleich?
Im europäischen Vergleich ist die Impfquote bei 15-jährigen Mädchen in Deutschland niedriger als in den meisten anderen Ländern.39 So lag Deutschland laut RKI und WHO 2019 bei den HPV-Impfquoten für eine vollständige Impfserie von 15-jährigen Mädchen in 25 europäischen Ländern nur auf dem 17. Platz (Abb. 4).40
Zu den europäischen Ländern mit den höchsten HPV-Impfquoten bei 15-jährigen Mädchen zählten 2019 Portugal (95 %), Island (88 %) und Norwegen (87 %).40
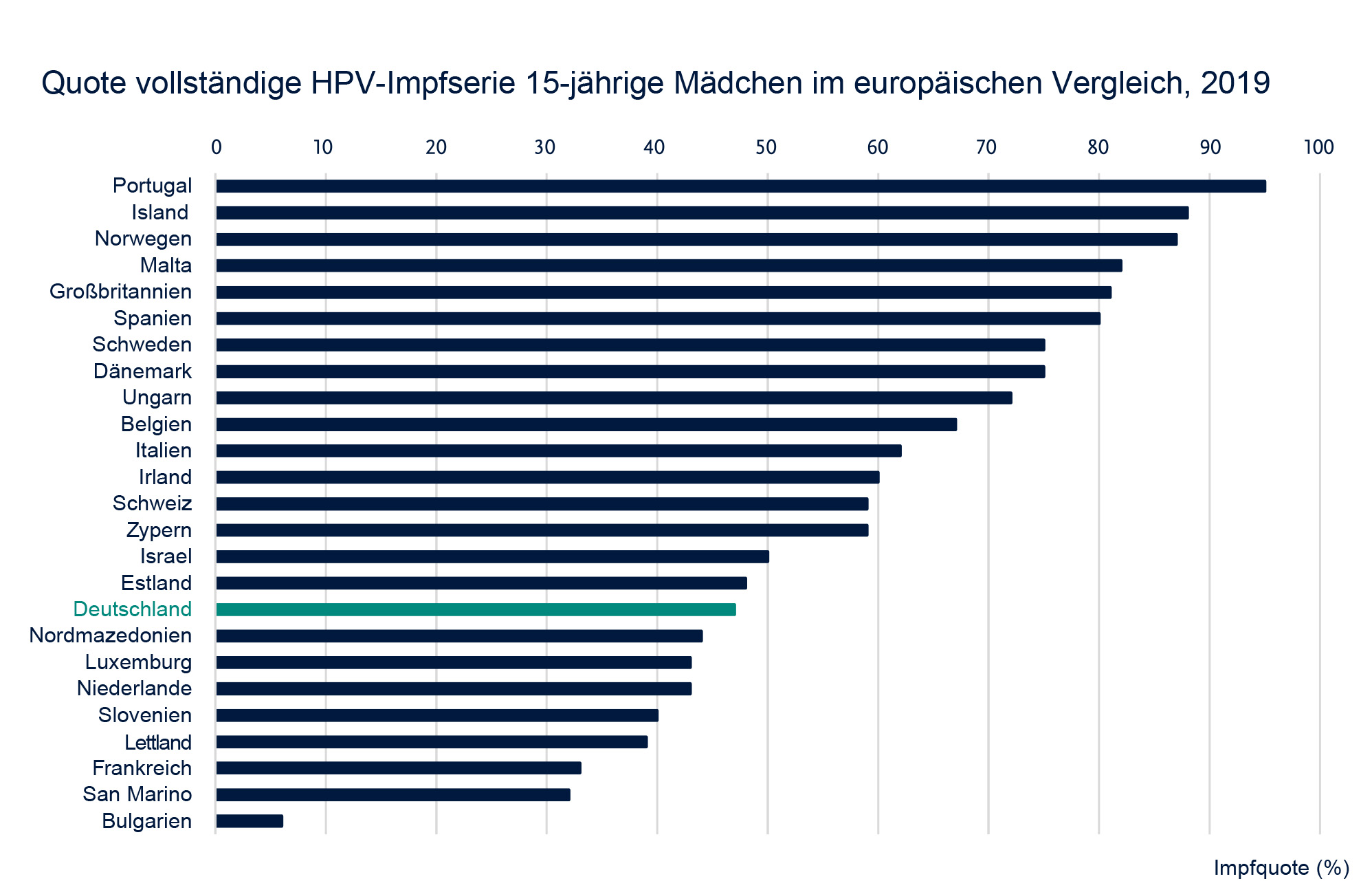
Abbildung 4: Impfquoten der 15-jährigen Mädchen mit vollständiger HPV-Impfserie im europäischen Vergleich für das Jahr 2019. Abbildung modifiziert von MSD.40
In Portugal wird eine allgemein große Akzeptanz für Impfungen in der Bevölkerung als Erklärung für die hohen Impfquoten gehandelt.14 Island und Norwegen haben die hohen Impfquoten durch schulbasierte Impfprogramme erzielt – auch Länder wie Schweden, Spanien oder das Vereinigte Königreich konnten durch Schulimpfprogramme Impfquoten von über 80 % erreichen.14
Auch im internationalen Vergleich zeigt sich ein Rückstand: Bezogen auf die Durchimpfung von 9- bis 14-jährigen Mädchen in einer Gruppe von 46 Ländern mit hohem Einkommen rangiert Deutschland bezüglich der HPV-Impfquote auf Rang 37.39
Niedrige Impfquoten sind auf das Fehlen von bevölkerungsbezogenen oder schulbasierten HPV-Impfprogrammen zurückzuführen.14 Für Deutschland sollte ein organisiertes oder schulbasiertes Programm für Mädchen und Jungen eingeführt werden, um eine Erhöhung der HPV-Impfquoten zu erreichen.14
Impfziel: HPV-Impfquoten bei Mädchen und Jungen erhöhen
Weltweit haben laut WHO gerade einmal 125 Länder (64 Prozent) die HPV-Impfung in ihr nationales Impfprogramm aufgenommen, in nur 47 Ländern (24 Prozent) sind die Jungen in die Impfempfehlung inkludiert.41 Schätzungen zufolge waren im Jahr 2019 weltweit nur 15 % der Mädchen und 4 % der Jungen vollständig gegen HPV geimpft.39
Sowohl die WHO als auch die EU haben sich einem Ziel verschrieben: Die Eliminierung des Zervix-Karzinoms.27, 42 Dafür ist u. a. eine Impfquote von 90 % für eine vollständige Impfung bei 15-jährigen Mädchen erforderlich.27, 42 Die EU geht hier noch darüber hinaus und erweitert dies noch um eine deutliche Erhöhung der Impfquoten bei Jungen.27 Deutschland ist eines der Länder, das sich den WHO und EU-Zielen verpflichtet hat.40
HPV-Impfquoten steigern: Ärzte in der Schlüsselrolle
HPV-Impfungen erfolgen vor allem bei niedergelassenen Kinderärzten, aber auch bei Allgemeinärzten, Gynäkologen und Urologen.14 Wie die Daten der Bundeszentrale für gesundheitliche Aufklärung (BZgA) zum Impfverhalten 2011 und 2014 darlegten, übernehmen Ärzte die Schlüsselrolle in der Impfberatung und Umsetzung der Impfempfehlung.43 Aus Überlegungen zur Erhöhung der HPV-Impfquote in Deutschland geht hervor, dass die Aufklärung dabei besonders im Fokus stehen sollte.38 So zeigte eine bevölkerungsbezogene Erhebung, dass nur 24,5 % der Erwachsenen in Deutschland von HPV gehört haben und nur 45 % von ihnen bekannt war, dass es Impfstoffe zur Vorbeugung einer HPV-Infektion gibt.38, 44
Sie können Ihren Teil zur Aufklärung über HPV und die HPV-Impfung beitragen! Helfen Sie dabei, die Impfquoten zu verbessern und Immunisierungen nachzuholen, sodass mehr Mädchen und Jungen sowie Frauen und Männer von einer Impfung zur Prävention von bestimmten HPV-bedingten Erkrankungen profitieren können. Sehen Sie sich daher unsere Maßnahmen-Liste an und machen Sie den Check!
Maßnahmen-Liste checken!
- Sprechen Sie die HPV-Impfung bei jeder Gelegenheit an und prüfen Sie den HPV-Impfstatus, unabhängig von Alter und Geschlecht Ihrer Patienten.
- Klären Sie über die mit einer HPV-Impfung verbundene Prävention von bestimmten HPV-bedingten Erkrankungen auf.
- Gehen Sie auf Bedenken aufgrund von Impf-Nebenwirkungen ein.
- Geben Sie klare Impfempfehlungen ab, denn Ihre Empfehlung kann den Unterschied machen.
- Führen Sie die HPV-Impfung zeitnah durch, am besten noch am selben Tag.
Viele gesetzliche und auch private Krankenversicherungen erstatten die Kosten für die HPV-Impfung auch für erwachsene Frauen und Männer.
Lesen Sie unsere Tipps für ein erfolgreiches HPV-Impfgespräch für Mädchen und Jungen.
Anmerkungen
#Europa = 31 Länder, für die die EMA (European Medicines Agency) zuständig ist, sowie die Schweiz. Die angegebenen Zahlen basieren auf einem Bericht zur Schätzung der jährlichen HPV-assoziierten Neuerkrankungen in Europa für das Jahr 2015. Die Schätzung basiert auf der Cancer Incidence in Five Continents (CI5) Volume X Datenbank der Jahre 2003–2007 der IARC (International Agency for Research on Cancer) sowie den Eurostat Population Data für 2015. Für die Schätzung der Inzidenz der Krebsvorstufen wurden Publikationen der Jahre 2004–2006 und 2009–2011 genutzt. Zur Schätzung der Inzidenz im Jahr 2015 wurden aktuelle Bevölkerungszahlen der genannten europäischen Länder herangezogen. Angegeben sind jeweils die in der Publikation geschätzte mittlere Anzahl an neuen HPV-assoziierten Karzinomen sowie die geschätzte Range der Anzahl an neuen HPV-assoziierten Krebsvorstufen und Genitalwarzen. Hier sind die Zahlen für Krebsarten und Krebsvorstufen angegeben, die durch alle HPV-Typen verursacht werden können.
*Gemessen an dem Wert der verlorenen Lebensjahre, “value of years of life lost” (VYLL)
Abkürzungen
BzgA: Bundeszentrale für gesundheitliche Aufklärung
EMA: European Medicines Agency
HPV: Humane Papillomviren
IARC: International Agency for Research on Cancer
KI: Konfidenzintervall
KV: Kassenärztliche Vereinigung
RKI: Robert Koch Institut
STIKO: Ständige Impfkommission
WHO: World Health Organization
Quellen
- Deutsches Krebsforschungszentrum (dkfz). Humane Papillomviren (HPV) als Krebs-Auslöser: Absteckung, Krebsrisiko, HPV Test; 2021 [eingesehen am 20.08.24]. Available from: URL: https://www.krebsinformationsdienst.de/vorbeugung/risiken/hpv2.php.
- RKI. RKI-Ratgeber Humane Papillomviren; Erstveröffentlichung im Epidemiologischen Bulletin 27/2018. Letzte Aktualisierungen: Abschnitt „Vorkommen“ vom Dezember 2023 [eingesehen am 20.08.24]. Available from: URL: https://www.rki.de/DE/Aktuelles/Publikationen/RKI-Ratgeber/Ratgeber/Ratgeber_HPV.html?nn=16906560.
- Fachinformation GARDASIL®. Stand September 2006.
- Paul-Ehrlich-Institut. HPV-Impfstoffe (humane Papillomaviren); 2024 [eingesehen am 27.08.24]. Available from: URL: https://www.pei.de/DE/arzneimittel/impfstoffe/gebaermutterhalskrebs-hpv/hpv-node.html.
- Bruni L et al. Cervical human papillomavirus prevalence in 5 continents: meta-analysis of 1 million women with normal cytological findings. J Infect Dis 2010; 202(12):1789–99.
- Zentrum für Krebsregisterdaten. Gebärmutterhalskrebs (Zervixkarzinom) [eingesehen am 20.08.24]. Available from: URL: https://www.krebsdaten.de/Krebs/DE/Content/Krebsarten/Gebaermutterhalskrebs/gebaermutterhalskrebs_node.html.
- Hartwig S et al. Estimation of the overall burden of cancers, precancerous lesions, and genital warts attributable to 9-valent HPV vaccine types in women and men in Europe. Infect Agent Cancer 2017; 12:19.
- Robert Koch-Institut (RKI). Ständige Impfkommission: Empfehlungen der Ständigen Impfkommission (STIKO) beim Robert Koch-Institut 2024: Epid Bull 2024;4:1- 72.
- Fachinformation GARDASIL® 9: Stand März 2024.
- Bencina G et al. Burden and indirect cost of vaccine-preventable cancer mortality in Europe. J Med Econ 2024; 27(sup2):30–40.
- Robert Koch-Institut. Antworten auf häufig gestellte Fragen (FAQ) zu Erreger und Impfung [eingesehen am 17.05.24]. Available from: URL: https://www.rki.de/SharedDocs/FAQs/DE/Impfen/HPV/FAQ-Liste_HPV_Impfen.html.
- Fachinformation Cervarix®. Stand Oktober 2021.
- Fachinformation GARDASIL® Stand März 2024.
- Osmani V KSJ. Bundesgesundheitsblatt – Gesundheitsforschung – Gesundheitsschutz.: 2021; 64: 590–599.
- zur Hausen H. Human papillomaviruses and their possible role in squamous cell carcinomas. Curr Top Microbiol Immunol 1977; 78:1–30.
- Wojcinski M. 14 Jahre HPV-Impfung: was haben wir erreicht? Gynakologe 2021; 54(11):801–9.
- Fachinformation GARDASIL®. Stand August 2010.
- Fachinformation GARDASIL®. Stand Juni 2014.
- Robert Koch-Institut (RKI). Epidemiologisches Bulletin. Epid Bull 2016; 16.
- Fachinformation Cervarix®. Stand September 2007.
- Fachinformation Cervarix®. Stand Dezember 2013.
- Fachinformation Cervarix®. Stand Juli 2016.
- Robert Koch-Institut (RKI). Epidemiologisches Bulletin. Epid Bull 2007; (12):97–106.
- Robert Koch-Institut (RKI). Epidemiologisches Bulletin. Epid Bull 2014; (35):341-350.
- Robert Koch-Institut (RKI). Epidemiologisches Bulletin. Epid Bull 2018; (35):383-390.
- World Health Organisation. Reaching 2030 cervical cancer elimination targets – New WHO recommendations for screening and treatment of cervical pre-cancer; 2021 [eingesehen am 20.08.24]. Available from: URL: https://www.who.int/news-room/events/detail/2021/07/06/default-calendar/reaching-2030-cervical-cancer-elimination-targets.
- Europäische Kommission. Europas Plan gegen den Krebs: Neue Maßnahmen für einen besseren Zugang zu Prävention, Früherkennung, Behandlung und Versorgung bei Krebs 2022; 2022 [eingesehen am 20.08.24]. Available from: URL: https://ec.europa.eu/commission/presscorner/detail/de/ip_22_702.
- MSD. Interne Daten.
- Gemeinsamer Bundesausschuss (GBA). Richtlinie über Schutzimpfungen (Stand März 2024) [eingesehen am 20.08.24]. Available from: URL: https://www.g-ba.de/richtlinien/60/.
- Debeka BKK. Schutzimpfungen [eingesehen am 20.08.24]. Available from: URL: https://www.debeka-bkk.de/leistungen-und-services/leistungen-a-z/schutzimpfungen/.
- Kassenärztliche Vereinigung Niedersachsen. Vereinbarung über die Durchführung von HPV-Impfungen als Satzungsleistung mit der AOK Niedersachsen (AOKN) [eingesehen am 20.08.24]. Available from: URL: https://www.kvn.de/Mitglieder/Rundschreiben/KVN+Rundschreiben+Dezember+2023/Vereinbarung+%C3%BCber+die+Durchf%C3%BChrung+von+HPV_Impfungen+als+Satzungsleistung+mit+der+AOK+Niedersachsen+%28AOKN%29-p-29282.html.
- IKK BB. HPV-Impfung [eingesehen am 20.08.24]. Available from: URL: https://www.ikkbb.de/leistungen/vorsorge/impfungen/hpv-impfung.
- Lei J et al. HPV Vaccination and the Risk of Invasive Cervical Cancer. N Engl J Med 2020; 383(14):1340–8.
- Kjaer SK et al. Real-World Effectiveness of Human Papillomavirus Vaccination Against Cervical Cancer. J Natl Cancer Inst 2021; 113(10):1329–35.
- Osmani V et al. HPV vaccination leads to decrease of anogenital warts and precancerous lesions of the cervix uteri in young women with low vaccination rates: a retrospective cohort analysis. BMC Cancer 2022; 22(1):1293.
- Grieger P et al. Erste Hinweise auf einen möglichen Effekt der HPV-Impfung auf die Krebsinzidenz in Deutschland: Zervixkarzinome im Fokus. Deutsches Ärzteblatt 2024 Jun 28.
- Rieck T et al. Impfquoten von Kinderschutzimpfungen in Deutschland – aktuelle Ergebnisse aus der RKI-Impfsurveillance: Epid Bull 2022;48:3-25.
- Wähner C et al. Uptake of HPV vaccination among boys after the introduction of gender-neutral HPV vaccination in Germany before and during the COVID-19 pandemic. Infection 2023:1–12.
- Bruni L et al. HPV vaccination introduction worldwide and WHO and UNICEF estimates of national HPV immunization coverage 2010-2019. Prev Med 2021; 144:106399.
- Takla A et al. Schulimpfprogramme als Lösung zur Steigerung der HPV-Impfquoten in Deutschland? – Entwicklung der Impfquoten in einer hessischen Modellregion mit Schulimpfprogramm, Epid Bull 2022;20:3-11.
- World Health Organization (WHO). Human papillomavirus vaccines: WHO position paper (2022 update) [eingesehen am 20.08.24]. Available from: URL: https://iris.who.int/bitstream/handle/10665/365350/WER9750-eng-fre.pdf?sequence=1.
- World Health Organization (WHO). Global strategy to accelerate the elimination of cervical cancer as a public health problem [eingesehen am 27.08.24]. Available from: URL: https://iris.who.int/bitstream/handle/10665/336583/9789240014107-eng.pdf?sequence=1.
- Stark S, Rodemerk H, Dornhöfer N, Hösemann C. HPV-Impfung in Deutschland: Aktueller Stand und Herausforderungen [eingesehen am 20.08.24]. Available from: URL: https://www.slaek.de/media/dokumente/ueber-uns/presse/aerzteblatt/archiv/2021-2030/2024/04/0424_023.pdf.
- Sharma SJ et al. Awareness of Human Papillomavirus (HPV) and HPV Vaccination amongst the General Population in Germany: Lack of Awareness and Need for Action. Oncol Res Treat 2022; 45(10):561–7.
DE-GSL-00302 09/24
