Studie: KEYNOTE-048
5-Jahres-Langzeitdaten beim M/uR HNSCC: Anhaltender Überlebensvorteil unter KEYTRUDA® in der Erstlinie
KEYTRUDA® (Pembrolizumab) ist als Monotherapie oder in Kombination mit Platin- und 5-Fluorouracil (5-FU)-Chemotherapie zur Erstlinienbehandlung des metastasierenden oder nicht resezierbaren rezidivierenden Plattenepithelkarzinoms der Kopf-Hals-Region (HNSCC) bei Erwachsenen mit PD-L1-exprimierenden Tumoren (CPS ≥ 1) angezeigt.1

Ziel der Studie
Die Studie KEYNOTE-048 untersuchte KEYTRUDA® bei Patienten mit metastasierendem oder nicht resezierbarem rezidivierenden HNSCC, die als nicht heilbar durch lokale Therapien galten. Die Wirksamkeit wurde bei allen Patienten unabhängig von der PD-L1-Expression untersucht und zusätzlich bei den Patienten mit einer PD-L1-Expression von einem Combined Positive Score (CPS) ≥ 1 und ≥ 20. Weiterhin untersuchte eine explorative Post-hoc-Analyse zur Therapiesequenz, ob Patienten mit PD-L1 CPS ≥ 1, die mit KEYTRUDA®-Monotherapie oder KEYTRUDA® in Kombination mit Chemotherapie in Erstlinie und danach mit einer Cetuximab-basierten Zweitlinientherapie vs. EXTREME in 1L und Immuntherapie in 2L behandelt wurden, profitieren können.2
KEYTRUDA® ist als Monotherapie oder in Kombination mit Platin- und 5-Fluorouracil (5-FU)-Chemotherapie zur Erstlinienbehandlung des metastasierenden oder nicht resezierbaren rezidivierenden Plattenepithelkarzinoms der Kopf-Hals-Region bei Erwachsenen mit PD-L1-exprimierenden Tumoren (Combined Positive Score [CPS] ≥ 1) angezeigt.1
Wichtige Ergebnisse auf einen Blick
Die Ergebnisse der zulassungsrelevanten Analyse der Studie KEYNOTE-048 ergaben bei erwachsenen Patienten mit metastasierendem oder nicht resezierbarem rezidivierenden Plattenepithelkarzinom der Kopf-Hals-Region, deren Tumore PD-L1 exprimierten, in der Erstlinienbehandlung nach einer medianen Nachbeobachtungszeit von 13,0 Monaten im KEYTRUDA®-Kombinationsarm bzw. 11,5 Monaten im KEYTRUDA®-Monotherapiearm (Datenschnitt 25.02.19):1,3
KEYTRUDA®-Monotherapie vs. EXTREME
KEYTRUDA® + Chemotherapie vs. EXTREME
OS unter KEYTRUDA®-Monotherapie vs. EXTREME* mit nachfolgender 2L-Therapie für den KEYTRUDA®-Einsatz in der palliativen 1L
Kann durch eine Optimierung der Therapiesequenz der Behandlungserfolg beeinflusst werden? Die Ergebnisse einer explorativen Post-hoc-Analyse der Studie KEYNOTE-048 unterstreichen den Stellenwert von KEYTRUDA® beim M/uR HNSCC sowohl als Monotherapie als auch in Kombination mit Chemotherapie zur Erstlinienbehandlung bei Patienten mit PD-L1-CPS ≥ 1. In der explorativen Post-hoc-Analyse mit einer medianen Nachbeobachtungszeit von 69,7 Monaten± zeigte sich bei Patienten mit PD-L1 CPS ≥ 1, die nach einer KEYTRUDA®-Monotherapie in der Erstlinie auf eine Cetuximab-basierte Therapie eingestellt wurden (n = 63):2
- eine Hazard-Ratio [HR] von 1,0 (95 %-Konfidenzintervall [KI]: 0,7–1,5) unter KEYTRUDA®-Monotherapie und darauffolgender Cetuximab-basierter Therapie.
- ein medianes Gesamtüberleben (OS) von 15,7 Monaten (95 %-KI: 12,3–22,6) vs. 16,5 Monaten (95 %-KI: 13,5–19,8) bei Patienten, die nach EXTREME* mit einer Immuntherapie behandelt wurden (n = 70).
- Das OS war damit bei Patienten, die nach einer KEYTRUDA®-Monotherapie eine Cetuximab-basierte Therapie erhielten, vergleichbar mit Patienten, die nach EXTREME* auf eine Immuntherapie umgestellt wurden.
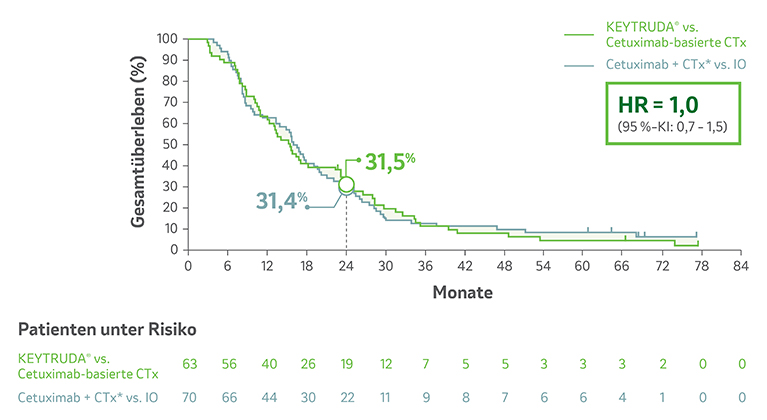
Abb. 1: Kaplan-Meier-Kurven zum Gesamtüberleben von Patienten, deren Tumore PD-L1 exprimierten (CPS ≥ 1) und die in der Erstlinie mit KEYTRUDA®-Monotherapie oder EXTREME und entsprechender nachfolgender Cetuximab-basierter Zweitlinientherapie in der Studie KEYNOTE-048 behandelt wurden, nach einer medianen Nachbeobachtungszeit von 69,7 Monaten±. Grafik erstellt von MSD nach Daten von Greil R et al. 2023.2
OS unter KEYTRUDA® plus Chemotherapie vs. EXTREME* mit nachfolgender 2L-Therapie für den KEYTRUDA®-Einsatz in der palliativen 1L
In der explorativen Post-hoc-Analyse der Therapiesequenz der Studie KEYNOTE-048 wurde nach einer medianen Nachbeobachtungszeit von 69,7 Monaten±± bei Patienten mit PD-L1 CPS ≥ 1 unter KEYTRUDA® plus Chemotherapie (n = 37) vs. EXTREME (n = 64) in der Erstlinie und nachfolgender Cetuximab-basierter Zweitlinientherapie beobachtet:2
- eine 30%-ige Reduktion des Sterberisikos (HR = 0,70; 95 %-KI: 0,4–1,0).
- Das mediane OS betrug 22,1 Monate (95 %-KI: 14,0–24,7) unter KEYTRUDA® plus Chemotherapie in der Erstlinie vs. 16,5 Monate (95 %-KI: 11,5–19,8) unter EXTREME in der Erstlinie.

Abb. 2: Kaplan-Meier-Kurven zum Gesamtüberleben von Patienten, deren Tumore PD-L1 exprimierten (CPS ≥ 1) und die in der Erstlinie mit KEYTRUDA® plus Chemotherapie oder EXTREME und entsprechender nachfolgender Cetuximab-basierter Zweitlinientherapie in der Studie KEYNOTE-048 behandelt wurden, nach einer medianen Nachbeobachtungszeit von 69,7 Monaten±±. Grafik erstellt von MSD nach Daten von Greil R et al. 2023.2
5-Jahres-Daten Monotherapie (PD-L1 CPS ≥ 1) Primärer Endpunkt Gesamtüberleben
Anhaltender Überlebensvorteil unter KEYTRUDA®-Monotherapie vs. EXTREME bei Patienten mit PD-L1-Expression (CPS ≥ 1) in der Studie KEYNOTE-0481,4
Das 5-Jahres-Update der Studie KEYNOTE-048 mit einer medianen Nachbeobachtungszeit von 69,2 Monaten (Spanne: 61,2–81,6; Datenschnitt: 21.02.2022) zeigte konsistent zu den zulassungsrelevanten Studienergebnissen einen anhaltenden Überlebensvorteil bei Patienten mit PD-L1-Expression (CPS ≥ 1) unter KEYTRUDA®-Monotherapie gegenüber EXTREME.4
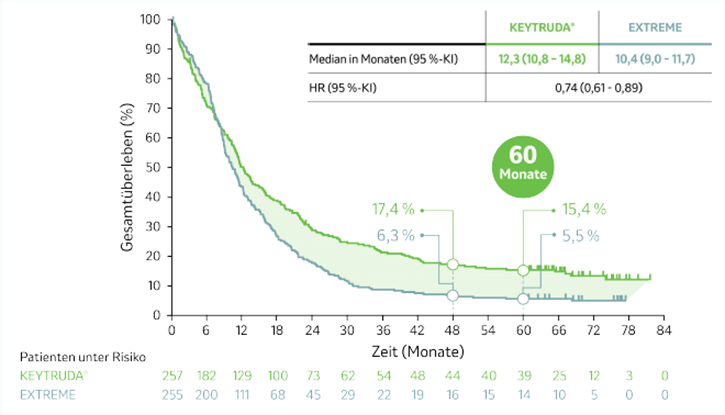
Abb. 3: Kaplan-Meier-Kurven zum Gesamtüberleben von Patienten, deren Tumore PD-L1 exprimierten (CPS ≥ 1) und die mit KEYTRUDA®-Monotherapie oder EXTREME in der Studie KEYNOTE-048 behandelt wurden, nach einer medianen Nachbeobachtungszeit von 69,2 Monaten (Datenschnitt 21.02.2022). Grafik erstellt von MSD nach Daten von Tahara et al. 2022.4
Sekundärer Endpunkt Objektive Ansprechrate (ORR)
Nach einer medianen Nachbeobachtungszeit von 69,2 Monaten wurden unter KEYTRUDA®-Monotherapie vs. EXTREME bei Patienten mit PD-L1-Expression (CPS ≥ 1) folgende objektive Ansprechraten erreicht:

Abb. 4: Balkendiagramm zur objektiven Ansprechrate von Patienten, deren Tumore PD-L1 exprimierten (CPS ≥ 1) und die mit KEYTRUDA®-Monotherapie oder EXTREME in der Studie KEYNOTE-048 behandelt wurden, nach einer medianen Nachbeobachtungszeit von 69,2 Monaten (Datenschnitt 21.02.2022). Grafik erstellt von MSD nach Daten von Tahara et al., 2022.4
Explorativer Endpunkt Dauer des Ansprechens (DOR£)
Das 5-Jahres-Update ergab weiterhin eine mehr als 5x längere mediane Dauer des Ansprechens (DOR£) unter KEYTRUDA®-Monotherapie gegenüber EXTREME:
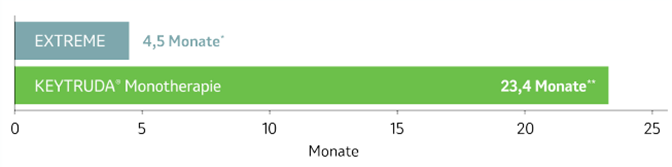
Abb. 5: Balkendiagramm zur Dauer des Ansprechens£ von Patienten, deren Tumore PD-L1 exprimierten (CPS ≥ 1) und die mit KEYTRUDA®-Monotherapie oder EXTREME in der Studie KEYNOTE-048 behandelt wurden, nach einer medianen Nachbeobachtungszeit von 69,2 Monaten (Datenschnitt 21.02.2022). Grafik erstellt von MSD nach Daten von Tahara et al., 2022.4
*Bereich 1,2+ bis 73,9+
**Bereich 1,5+ bis 75,5+
5-Jahres-Daten Monotherapie (PD-L1 CPS ≥ 20)
Primärer Endpunkt Gesamtüberleben
Anhaltender Überlebensvorteil unter KEYTRUDA®-Monotherapie vs. EXTREME bei Patienten mit hoher PD-L1-Expression (CPS ≥ 20) in der KEYNOTE-0481,4
Das 5-Jahres-Update der Studie KEYNOTE-048 bestätigte vorherige zulassungsrelevante Studienergebnisse und zeigte auch bei Patienten mit hoher PD-L1-Expression (CPS ≥ 20) einen anhaltenden Überlebensvorteil nach einer medianen Nachbeobachtungszeit von 69,2 Monaten (Spanne: 61,2–81,6; Datenschnitt: 21.02.2022) unter KEYTRUDA®-Monotherapie gegenüber EXTREME.4
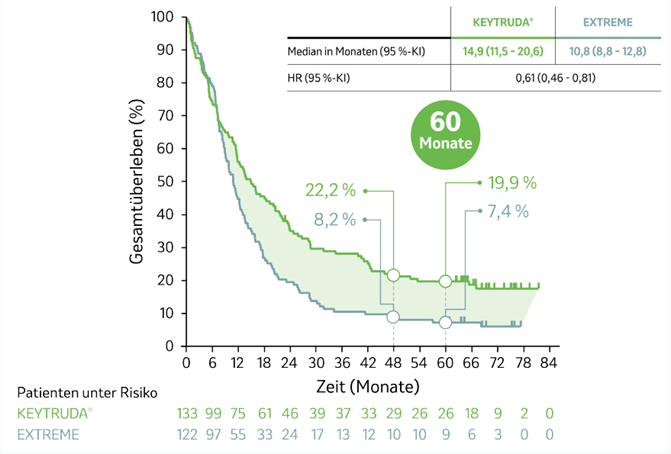
Abb. 6: Kaplan-Meier-Kurven zum Gesamtüberleben von Patienten, deren Tumore eine hohe PD-L1-Expression (CPS ≥ 20) aufwiesen und die mit KEYTRUDA®-Monotherapie oder EXTREME in der Studie KEYNOTE-048 behandelt wurden, nach einer medianen Nachbeobachtungszeit von 69,2 Monaten (Datenschnitt 21.02.2022). Grafik erstellt von MSD nach Daten von Tahara et al., 2022.4
Sekundärer Endpunkt Objektive Ansprechrate
Nach einer medianen Nachbeobachtungszeit von 69,2 Monaten wurden unter KEYTRUDA®-Monotherapie vs. EXTREME bei Patienten mit PD-L1-Expression (CPS ≥ 20) folgende objektive Ansprechraten erreicht:
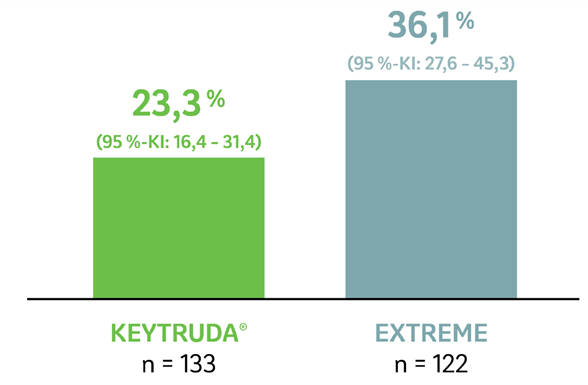
Abb. 7: Balkendiagramm zur objektiven Ansprechrate von Patienten, deren Tumore PD-L1 exprimierten (CPS ≥ 20) und die mit KEYTRUDA®-Monotherapie oder EXTREME in der Studie KEYNOTE-048 behandelt wurden, nach einer medianen Nachbeobachtungszeit von 69,2 Monaten (Datenschnitt 21.02.2022). Grafik erstellt von MSD nach Daten von Tahara et al., 2022.4
Explorativer Endpunkt Dauer des Ansprechens (DOR£)
Das 5-Jahres-Update ergab weiterhin eine mehr als 5x längere mediane DOR£ unter KEYTRUDA®-Monotherapie gegenüber EXTREME:
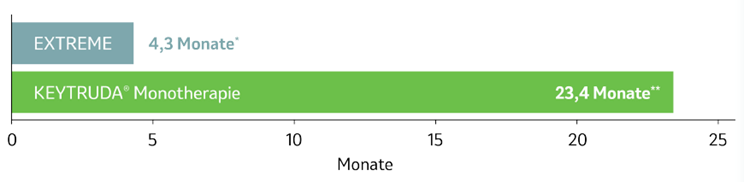
Abb. 8: Balkendiagramm zur Dauer des Ansprechens£ von Patienten, deren Tumore eine hohe PD-L1-Expression (CPS ≥ 20) aufwiesen und die mit KEYTRUDA®-Monotherapie oder EXTREME in der Studie KEYNOTE-048 behandelt wurden, nach einer medianen Nachbeobachtungszeit von 69,2 Monaten (Datenschnitt 21.02.2022). Grafik erstellt von MSD nach Daten von Tahara et al., 2022.4
*Bereich 1,2+ bis 38,2+
**Bereich 2,7+ bis 75,5+
Sicherheitsdaten nach einer medianen Nachbeobachtungszeit von 69,2 Monaten (Spanne: 61,2 – 81,6) unter KEYTRUDA®-Monotherapie
Das Sicherheitsprofil der KEYTRUDA®-Monotherapie war konsistent mit dem bekannten Sicherheitsprofil aus vorangegangenen Analysen.4
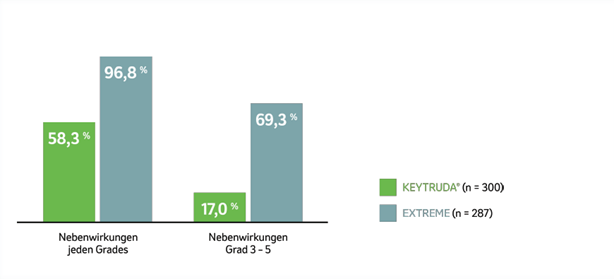
Abb. 9: Balkendiagramm zum Auftreten von Nebenwirkungen bei Patienten, die mit KEYTRUDA® als Monotherapie mit EXTREME in der Studie KEYNOTE-048 behandelt wurden, nach einer medianen Nachbeobachtungszeit von 69,2 Monaten (Datenschnitt 21.02.2022). Grafik erstellt von MSD nach Daten von Tahara et al., 2022.4
5-Jahres-Daten Kombinationstherapie (PD-L1 CPS ≥ 1)
Primärer Endpunkt Gesamtüberleben
Anhaltender Überlebensvorteil unter KEYTRUDA® plus Chemotherapie vs. EXTREME bei Patienten mit PD-L1-Expression (CPS ≥ 1) in der KEYNOTE-0481,4
Das 5-Jahres-Update der Studie KEYNOTE-048 zeigte einen anhaltenden Überlebensvorteil bei Patienten mit PD-L1-Expression (CPS ≥ 1) nach einer medianen Nachbeobachtungszeit von 68,6 Monaten (Spanne: 61,2—82,1 Monate, Datenschnitt: 21.02.2022) unter KEYTRUDA® plus Chemotherapie gegenüber EXTREME.3
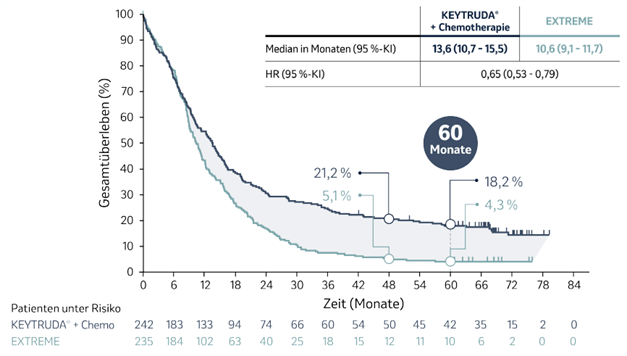
Abb. 10: Kaplan-Meier-Kurven zum Gesamtüberleben von Patienten, deren Tumore PD-L1 (CPS ≥ 1) exprimierten und die mit KEYTRUDA® plus Chemotherapie oder EXTREME in der Studie KEYNOTE-048 behandelt wurden, nach einer medianen Nachbeobachtungszeit von 68,6 Monaten (Datenschnitt 21.02.22). Grafik erstellt von MSD nach Daten von Tahara et al., 2022.4
Sekundärer Endpunkt Objektive Ansprechrate
Nach einer medianen Nachbeobachtungszeit von 68,6 Monaten wurden unter KEYTRUDA® plus Chemotherapie vs. EXTREME bei Patienten mit PD-L1-Expression (CPS ≥ 1) folgende objektive Ansprechraten erreicht:

Abb. 11: Balkendiagramm zur objektiven Ansprechrate von Patienten, deren Tumore PD-L1 exprimierten (CPS ≥ 1) und die mit KEYTRUDA® plus Chemotherapie oder EXTREME in der Studie KEYNOTE-048 behandelt wurden, nach einer medianen Nachbeobachtungszeit von 68,6 Monaten (Datenschnitt 21.02.2022). Grafik erstellt von MSD nach Daten von Tahara et al., 2022.4
Explorativer Endpunkt Dauer des Ansprechens£
Das 5-Jahres-Update ergab weiterhin eine mehr als 50 % längere mediane Dauer des Ansprechens (DOR£) unter KEYTRUDA® plus Chemotherapie gegenüber EXTREME:
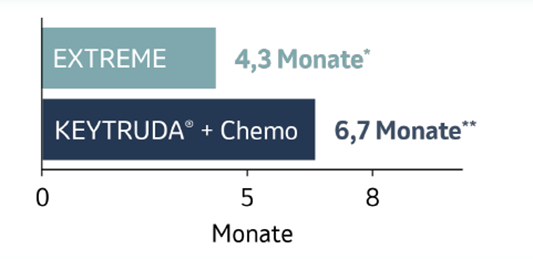
Abb. 12: Balkendiagramm zur Dauer des Ansprechens£ von Patienten, deren Tumore PD-L1 (CPS ≥ 1) exprimierten und die mit KEYTRUDA® plus Chemotherapie oder EXTREME in der Studie KEYNOTE-048 behandelt wurden, nach einer medianen Nachbeobachtungszeit von 68,6 Monaten (Datenschnitt 21.02.2022). Grafik erstellt von MSD nach Daten von Tahara et al., 2022.4
*Bereich 1,2+ bis 66,5+
**Bereich 1,6+ bis 73,8+
5-Jahres-Daten Kombinationstherapie (PD-L1 CPS ≥ 20)
Primärer Endpunkt Gesamtüberleben
Anhaltender Überlebensvorteil unter KEYTRUDA® plus Chemotherapie vs. EXTREME bei Patienten mit hoher PD-L1-Expression (CPS ≥ 20) in der KEYNOTE-0481,4
Das 5-Jahres-Update der Studie KEYNOTE-048 bestätigte vorherige zulassungsrelevante Studienergebnisse und zeigte einen anhaltenden Überlebensvorteil bei Patienten mit hoher PD-L1-Expression (CPS ≥ 20) nach einer medianen Nachbeobachtungszeit von 68,6 Monaten (61,2–82,1 Monate, Datenschnitt: 21.02.2022) unter KEYTRUDA® plus Chemotherapie gegenüber EXTREME.4

Abb. 13: Kaplan-Meier-Kurven zum Gesamtüberleben von Patienten, deren Tumore eine hohe PD-L1-Expression (CPS ≥ 20) aufwiesen und die mit KEYTRUDA® plus Chemotherapie oder EXTREME in der Studie KEYNOTE-048 behandelt wurden, nach einer medianen Nachbeobachtungszeit von 68,6 Monaten (Datenschnitt 21.02.2022). Grafik erstellt von MSD nach Daten von Tahara et al., 2022.4
Sekundärer Endpunkt Objektive Ansprechrate
Nach einer medianen Nachbeobachtungszeit von 68,6 Monaten wurden unter KEYTRUDA® plus Chemotherapie vs. EXTREME bei Patienten mit PD-L1-Expression (CPS ≥ 20) folgende objektive Ansprechraten erreicht:
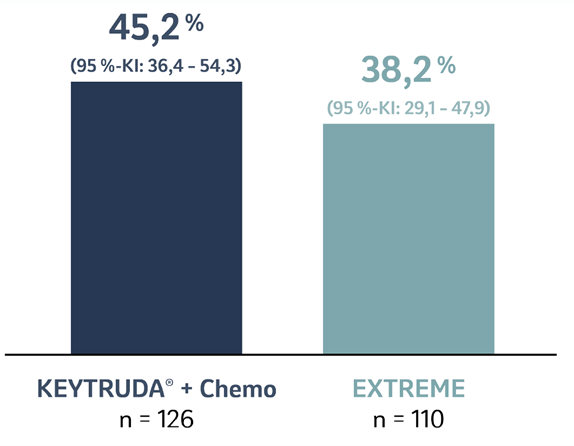
Abb. 14: Balkendiagramm zur objektiven Ansprechrate von Patienten, deren Tumore PD-L1 exprimierten (CPS ≥ 20) und die mit KEYTRUDA® plus Chemotherapie oder EXTREME in der Studie KEYNOTE-048 behandelt wurden, nach einer medianen Nachbeobachtungszeit von 68,6 Monaten (Datenschnitt 21.02.2022). Grafik erstellt von MSD nach Daten von Tahara et al., 2022.4
Explorativer Endpunkt Dauer des Ansprechens£
Das 5-Jahres-Update ergab weiterhin eine mehr als 50 % längere mediane DOR£ unter KEYTRUDA® plus Chemotherapie gegenüber EXTREME:
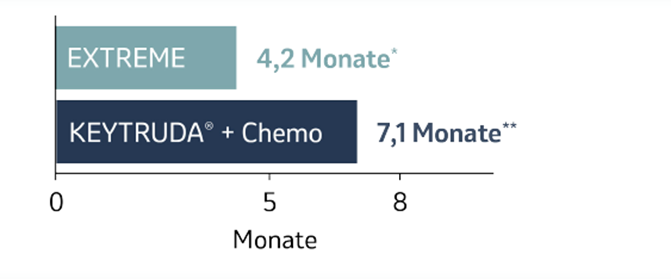
Abb. 15: Balkendiagramm zur Dauer des Ansprechens£ von Patienten, deren Tumore eine hohe PD-L1-Expression (CPS ≥ 20) aufwiesen und die mit KEYTRUDA® plus Chemotherapie oder EXTREME in der Studie KEYNOTE-048 behandelt wurden, nach einer medianen Nachbeobachtungszeit von 68,6 Monaten (Datenschnitt 21.02.2022). Grafik erstellt von MSD nach Daten von Tahara et al., 2022.4
*Bereich 1,2+ bis 38,2+
*Bereich 2,1+ bis 73,8+
Sicherheitsdaten nach einer medianen Nachbeobachtungszeit von 68,6 Monaten (61,2–82,1 Monate)
Das Sicherheitsprofil von KEYTRUDA® in Kombination mit Chemotherapie war konsistent mit dem bekannten Sicherheitsprofil. Das 5-Jahres-Update zeigte bei 69,3 % der Patienten unter EXTREME und 71,7 % der Patienten unter KEYTRUDA® plus Chemotherapie Nebenwirkungen vom Grad 3–5.4
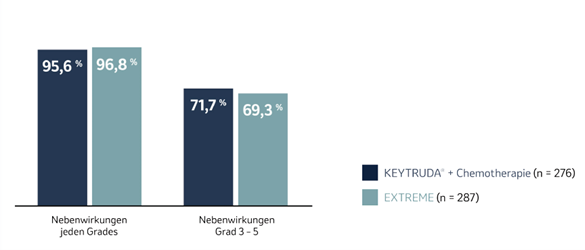
Abb. 16: Balkendiagramm zum Auftreten von Nebenwirkungen bei Patienten, die mit KEYTRUDA® plus Chemotherapie oder mit EXTREME in der Studie KEYNOTE-048 behandelt wurden, nach einer medianen Nachbeobachtungszeit von 68,6 Monaten (Datenschnitt 21.02.2022). Grafik erstellt von MSD nach Daten von Tahara et al., 2022.4
Die Studie KEYNOTE-048 war eine multizentrische, offene, randomisierte und aktiv kontrollierte Phase-3-Studie mit Patienten mit histologisch bestätigtem metastasierenden oder nicht resezierbaren rezidivierenden HNSCC ohne systemische Vorbehandlung der metastasierten Erkrankung, die durch lokale Therapie nicht mehr heilbar waren.1
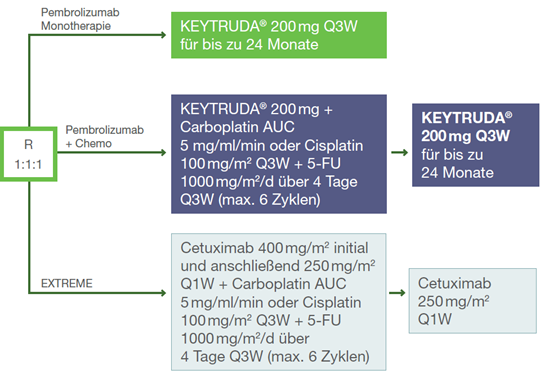
Abb.17: Studiendesign der Studie KEYNOTE-048. Grafik erstellt von MSD nach Daten von Burtness et al., 2019.3
Die Patienten (n = 882) wurden 1:1:1 randomisiert und nach PD-L1-Expression (TPS ≥ 50 % oder <50 %), HPV-Status (positiv oder negativ) sowie ECOG-Performance-Status (0 vs. 1) stratifiziert. Sie erhielten entweder:1
- KEYTRUDA® 200 mg alle 3 Wochen (Q3W; n = 301),
- KEYTRUDA® 200 mg Q3W plus Cisplatin 100 mg/m2 Q3W oder Carboplatin AUC 5 mg/ml/min Q3W plus 5-FU 1.000 mg/m2/d über 4 Tage Q3W über maximal 6 Zyklen gefolgt von KEYTRUDA® 200 mg Q3W (n = 281) oder
- Cetuximab 400 mg/m2 initial und anschließend 250 mg/m2 einmal die Woche (Q1W) plus Cisplatin 100 mg/m2 Q3W oder Carboplatin AUC 5 mg/ml/min Q3W plus 5-FU 1.000 mg/m2/d über 4 Tage Q3W für maximal 6 Zyklen gefolgt von Cetuximab 250 mg/m2 Q1W (n = 300).
Die Behandlung mit KEYTRUDA® wurde bis zum Fortschreiten der Erkrankung (beurteilt durch den Prüfarzt anhand RECIST-v1.1-Kriterien), bis zum Auftreten unzumutbarer Toxizität oder bis zu einer Maximaldauer von 24 Monaten fortgesetzt.
Ausschlusskriterien
Ausgeschlossen von der Studie waren unter anderem Patienten mit:
- einer aktiven Autoimmunerkrankung, die eine systemische Therapie innerhalb der letzten beiden Behandlungsjahre erforderte
- einer Erkrankung, die eine Immunsuppression erforderte.
Studienendpunkte
Primäre Wirksamkeitsendpunkte
- Gesamtüberleben
- Progressionsfreies Überleben (PFS)$
Sekundäre Wirksamkeitsendpunkte
- PFS-Raten$ nach 6 und 12 Monaten
- ORR$
- Veränderung der Lebensqualität seit Baseline und Zeit bis zur Verschlechterung der Lebensqualität
- Sicherheit und Verträglichkeit
Baseline-Patientencharakteristika der ITT-Population
KEYTRUDA® wurde in der Studie KEYNOTE-048 über ein breites Patientenkollektiv hinweg untersucht. Unter den 882 Patienten waren 754 Patienten (85 %), deren Tumore PD-L1 mit einem einen CPS ≥ 1 exprimierten und 381 (43 %) mit einem CPS ≥ 20.3
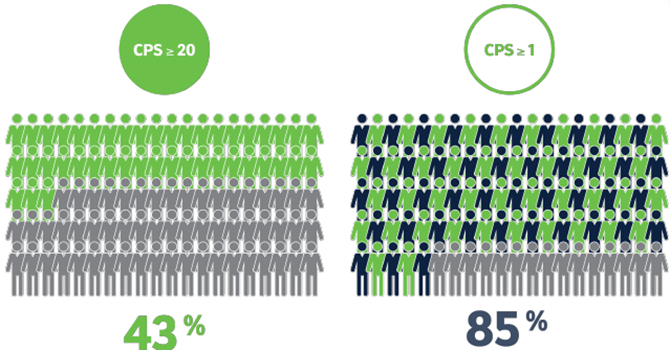
Abb.18: Schaubild, das den prozentualen Anteil von Patienten der Studie KEYNOTE-048 verdeutlicht, deren Tumore PD-L1 mit einem CPS ≥ 1 und einem CPS ≥ 20 exprimieren. Grafik erstellt von MSD nach Daten von Burtness et al., 2019.3
Darüber hinaus wurden folgende Charakteristika der Intention-to-treat (ITT)-Population zu Studienbeginn erfasst:
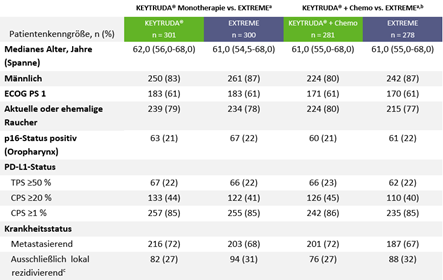
Tab.1: Patientencharakteristika der ITT-Population zu Studienbeginn. Tabelle modifiziert von MSD nach Daten von Burtness et al., 2019.3
a Patienten unter dem EXTREME-Regime erhielten Cetuximab plus Carboplatin plus 5-FU oder Cisplatin plus 5-FU, b enthält nur Studienteilnehmer, die in die EXTREME-Gruppe randomisiert wurden, während die Gruppe, die KEYTRUDA® plus Platin plus 5-FU zugeordnet war, offen für die Registrierung war, c lokal rezidivierend inkludierte Teilnehmer mit lokal rezidivierender Erkrankung sowie mit einer Ausbreitung auf zervikale Lymphknoten.
KEYTRUDA®-Monotherapie (PD-L1 CPS ≥ 1)
Primäre Endpunkte Gesamtüberleben und progressionsfreies Überleben
In der finalen Analyse der Studie KEYNOTE-048 zeigte sich nach 11,5 Monaten medianer Nachbeobachtungszeit unter KEYTRUDA®-Monotherapie vs. EXTREME bei Patienten mit PD-L1-Expression (CPS ≥ 1) ein signifikant verbessertes OS (HR: 0,74; 95 %-KI: 0,61 – 0,90; p = 0,00133‡) mit einem medianen OS von 12,3 Monaten (95 %-KI: 10,8 – 14,3) bzw. 10,3 Monaten (95 %-KI: 9,0–11,5) und ein vergleichbares progressionsfreies Überleben (HR: 1,13; 95 %-KI: 0,94–1,36; p = 0,89580‡) mit einem medianen PFS von 3,2 Monaten (95 %-KI: 2,2–3,4) bzw. 5,0 Monaten (95 %-KI: 4,8–6,0).1,3
Sekundärer Endpunkt Ansprechrate$
Bei Patienten, deren Tumore PD-L1 exprimierten (CPS ≥ 1) und die mit einer KEYTRUDA®-Monotherapie behandelt wurden, lag die ORR$ (CR+PR) bei 19,1 % (95 %-KI: 14,5–24,4; n = 49/257) gegenüber 35 % (95 %-KI: 29,1–41,1; n = 89/255) unter EXTREME.1,3
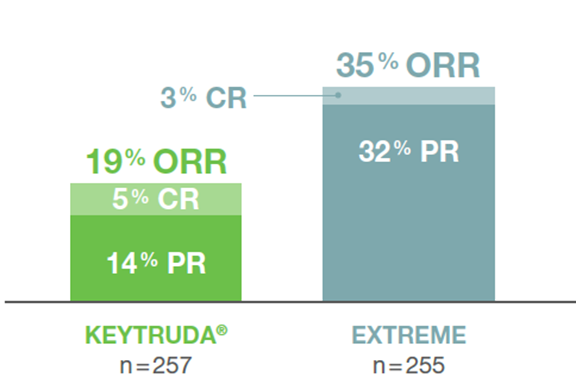
Abb. 19: Gesamtansprechrate von Patienten, deren Tumore PD-L1 exprimierten (CPS ≥ 1) und die mit KEYTRUDA®-Monotherapie oder EXTREME in der Studie KEYNOTE-048 behandelt wurden, nach einer medianen Nachbeobachtungszeit von 11,5 Monaten (Datenschnitt 25.02.19). Grafik erstellt von MSD nach Daten von Burtness et al., 2019.3
KEYTRUDA®-Monotherapie (PD-L1 CPS ≥ 20)
Primäre Endpunkte Gesamtüberleben und progressionsfreies Überleben
In der finalen Analyse der Studie KEYNOTE-048 zeigten sich nach 11,5 Monaten medianer Nachbeobachtungszeit unter KEYTRUDA®-Monotherapie vs. EXTREME bei Patienten mit hoher PD-L1-Expression (CPS ≥ 20) ein signifikant verbessertes OS (HR: 0,58; 95 %-KI: 0,44–0,78; p = 0,00010‡) mit einem medianen OS von 14,8 Monaten (95 %-KI: 11,5–20,6) bzw. 10,7 Monaten (95 %-KI: 8,8–12,8) und ein vergleichbares progressionsfreies Überleben (HR: 0,99; 95 %-KI: 0,76–1,29; p = 0,46791‡) mit einem medianen PFS von 3,4 Monaten (95 %-KI: 3,2–3,8) bzw. 5,3 Monaten (95 %-KI: 4,8–6,3).1,3
Sekundärer Endpunkt Ansprechrate$
Bei Patienten, deren Tumore eine hohe PD-L1-Expression (CPS ≥ 20) aufwiesen und die mit einer KEYTRUDA®-Monotherapie behandelt wurden, lag die ORR$ bei 23,3 % (95 %-KI: 16,4–31,4; n = 31/133) gegenüber 36,1 % (95 %-KI: 27,6–45,3; n = 44/122) unter EXTREME.1
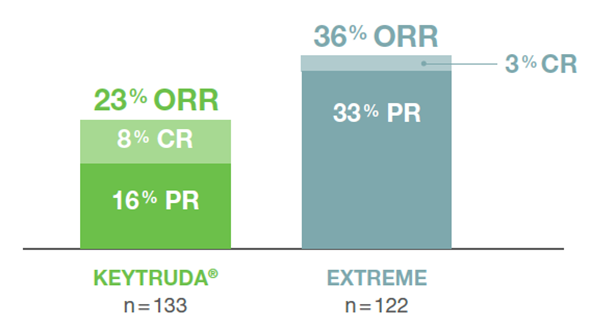
Abb. 20: Gesamtansprechrate von Patienten, deren Tumore eine hohe PD-L1-Expression (CPS ≥ 20) aufwiesen und die mit KEYTRUDA®-Monotherapie oder EXTREME in der Studie KEYNOTE-048 behandelt wurden, nach einer medianen Nachbeobachtungszeit von 11,5 Monaten (Datenschnitt 25.02.19). Grafik erstellt von MSD nach Daten von Burtness et al., 2019.3
Verträglichkeit in der Studie KEYNOTE-048 – KEYTRUDA®-Monotherapie
Günstigeres Sicherheitsprofil unter KEYTRUDA®-Monotherapie verglichen mit EXTREME in der Studie KEYNOTE-0483
Die Sicherheitsanalyse umfasste alle randomisierten Patienten, die mindestens eine Dosis KEYTRUDA® oder EXTREME erhalten hatten (As-treated-Population, n = 863). Zum Zeitpunkt der Analyse betrug die mediane Behandlungszeit 3,5 Monate (Interquartilsabstand¥ [IQR]: 1,4–7,6) unter KEYTRUDA®-Monotherapie und 4,9 Monate (IQR: 2,5–7,4) unter EXTREME. Die beobachteten unerwünschten Ereignisse entsprachen den bekannten Sicherheitsprofilen von KEYTRUDA® bzw. EXTREME.3
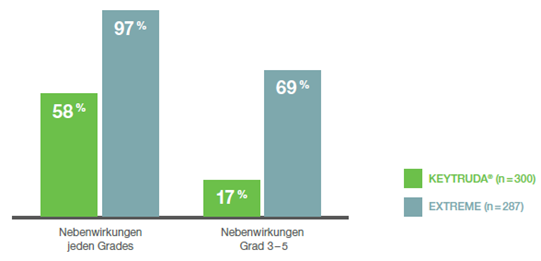
Abb. 21: Säulendiagramm aller Nebenwirkungen, die bei ≥ 10 % der Patienten der Studie KEYNOTE-048 auftraten, die mit KEYTRUDA®-Monotherapie oder EXTREME behandelt wurden, nach einer medianen Nachbeobachtungszeit von 11,5 Monaten (Datenschnitt 25.02.19). Grafik erstellt von MSD nach Daten von Burtness et al., 2019.3
Im Detail wurden folgende Nebenwirkungen aller Grade mit einer Inzidenz von ≥ 15 % unter KEYTRUDA®-Monotherapie vs. EXTREME beobachtet:
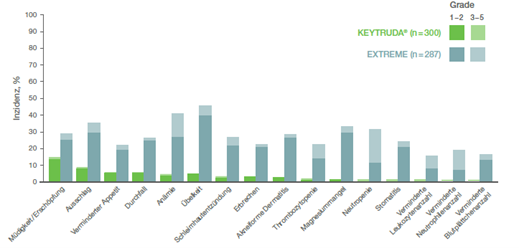
Abb. 22: Säulendiagramm mit Nebenwirkungen aller Grade, die bei ≥ 15 % der Patienten der Studie KEYNOTE-048 auftraten, die mit KEYTRUDA®-Monotherapie oder EXTREME behandelt wurden, nach einer medianen Nachbeobachtungszeit von 11,5 Monaten (Datenschnitt 25.02.19). Grafik erstellt von MSD nach Daten von Burtness et al., 2019.3
Weitere ausführliche Angaben zum Nebenwirkungsprofil von KEYTRUDA® über verschiedene Indikationen finden Sie in der Zusammenfassung des Sicherheitsprofils.
KEYTRUDA®-Kombinationstherapie (PD-L1 CPS ≥ 1)
Primäre Endpunkte Gesamtüberleben und progressionsfreies Überleben
In der finalen Analyse der Studie KEYNOTE-048 zeigten sich nach 13,0 Monaten medianer Nachbeobachtungszeit unter KEYTRUDA® plus Chemotherapie im Vergleich zu EXTREME bei Patienten mit PD-L1-Expression CPS ≥ 1 ein signifikant verbessertes OS (HR: 0,65; 95 %-KI: 0,53–0,80; p = 0,00002‡) mit einem medianen OS von 13,6 Monaten (95 %-KI: 10,7–15,5) bzw. 10,4 Monaten (95 %-KI: 9,1–11,7) und ein verbessertes progressionsfreies Überleben (HR: 0,84; 95 %-KI: 0,69–1,02; p = 0,03697‡) mit einem medianen PFS von 5,1 Monaten (95 %-KI: 4,7–6,2) bzw. 5,0 Monaten (95 %-KI: 4,8–6,0).1,3
Sekundärer Endpunkt Ansprechrate$
Bei Patienten, deren Tumore PD-L1 exprimierten (CPS ≥ 1), lag die ORR$ unter einer Kombinationstherapie aus KEYTRUDA® plus Chemotherapie und unter EXTREME bei 36 % (95 %-KI: 30,3–42,8; n = 88/242) vs. 36 % (95 %-KI: 29,6–42,2; n = 84/235).1

Abb. 23: Gesamtansprechrate von Patienten, deren Tumore PD-L1 exprimierten (CPS ≥ 1) und die mit KEYTRUDA® plus Chemotherapie oder EXTREME in der Studie KEYNOTE-048 behandelt wurden nach einer medianen Nachbeobachtungszeit von 13,0 Monaten (Datenschnitt 25.02.19). Grafik erstellt von MSD nach Daten von Burtness et al., 2019.3
KEYTRUDA®-Kombinationstherapie (PD-L1 CPS ≥ 20)
Primäre Endpunkte Gesamtüberleben und progressionsfreies Überleben
In der finalen Analyse der Studie KEYNOTE-048 zeigten sich nach 13,0 Monaten medianer Nachbeobachtungszeit unter KEYTRUDA® plus Chemotherapie im Vergleich zu EXTREME bei Patienten mit hoher PD-L1-Expression (CPS ≥ 20) ein signifikant verbessertes OS (HR: 0,60; 95 %-KI: 0,45–0,82; p = 0,00044‡) mit einem medianen OS von 14,7 Monaten (95 %-KI: 10,3–19,3) vs. 11,0 Monaten (95 %-KI: 9,2–13,0) sowie ein verbessertes progressionsfreies Überleben (HR: 0,76; 95 %-KI: 0,58–1,01; p = 0,02951‡) mit einem medianen PFS von 5,8 Monaten (95 %-KI: 4,7–7,6) bzw. 5,3 Monaten (95 %-KI: 4,9–6,3) .1,3
Sekundärer Endpunkt Ansprechrate$
Bei Patienten mit hoher PD-L1-Tumorexpression (CPS ≥ 20), die mit einer Kombinationstherapie aus KEYTRUDA® und Chemotherapie behandelt wurden, lag die ORR$ (CR + PR) bei 42,9 % (95 %-KI: 34,1–52,0; n = 54/126) gegenüber 38,2 % (95 %-KI: 29,1–47,9; n = 42/110) unter EXTREME.1
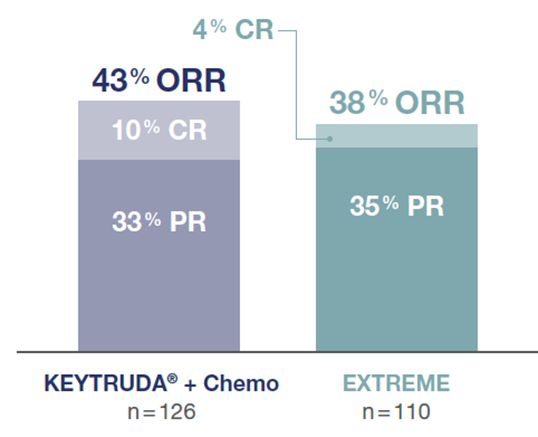
Abb. 24: Gesamtansprechrate von Patienten, deren Tumore eine hohe PD-L1-Expression (CPS ≥ 20) aufwiesen und die mit KEYTRUDA® plus Chemotherapie oder EXTREME in der Studie KEYNOTE-048 behandelt wurden, nach einer medianen Nachbeobachtungszeit von 13,0 Monaten (Datenschnitt 25.02.19). Grafik erstellt von MSD nach Daten von Burtness et al., 2019.3
Verträglichkeit in der Studie KEYNOTE-048 – KEYTRUDA®-Kombinationstherapie
Die Sicherheitsanalyse umfasste die As-treated-Population (n = 863). Zum Zeitpunkt der Analyse betrug die mediane Behandlungszeit 5,8 Monate (IQR¥: 2,8–9,7) unter KEYTRUDA® plus Chemotherapie und 4,9 Monate (IQR: 2,5–7,4) unter EXTREME. Die beobachteten unerwünschten Ereignisse entsprachen den bekannten Sicherheitsprofilen von KEYTRUDA® bzw. EXTREME.
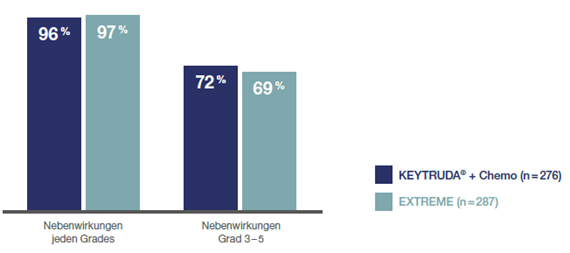
Abb. 25: Säulendiagramm aller Nebenwirkungen, die bei ≥ 10 % der Patienten der Studie KEYNOTE-048 auftraten, die mit KEYTRUDA® plus Chemotherapie oder EXTREME behandelt wurden, nach einer medianen Nachbeobachtungszeit von 13,0 Monaten (Datenschnitt 25.02.19). Grafik erstellt von MSD nach Daten von Burtness et al., 2019.3

Abb. 26: Säulendiagramm mit Nebenwirkungen aller Grade, die bei ≥ 15 % der Patienten der Studie KEYNOTE-048 auftraten, die mit KEYTRUDA® plus Chemotherapie oder EXTREME behandelt wurden, nach einer medianen Nachbeobachtungszeit von 13,0 Monaten (Datenschnitt 25.02.19). Grafik erstellt von MSD nach Daten von Burtness et al., 2019.3
Weitere ausführliche Angaben zum Nebenwirkungsprofil von KEYTRUDA® über verschiedene Indikationen finden Sie in der Zusammenfassung des Sicherheitsprofils.
Weiterlesen
Eine Testung von HNSCC-Tumoren auf eine PD-L1-Expression kann der Schlüssel sein, um Ihren Patienten Perspektiven in der Behandlung zu eröffnen. In der Regel dauert die PD-L1-Testung 3 Tage an. So können Sie Ihren geeigneten Patienten mit bestimmten fortgeschrittenen Kopf-Hals-Tumoren weitere Möglichkeiten anbieten. Finden Sie hier heraus, wie das geht.
Anmerkungen
* EXTREME: Cetuximab + [Carboplatin oder Cisplatin] + 5-FU
‡ HR basierend auf dem Stratified-Cox-Proportional-Hazardmodell, p-Wert basierend auf dem stratifizierten Log-Rank-Test
£ Explorativer Endpunkt; basierend auf Kaplan-Meier-Schätzungen
± Mediane Nachbeobachtungszeit: 69,7 Monate (Spanne: 61,4 bis 80,1) unter KEYTRUDA®-Monotherapie und 67,5 Monate (Spanne: 61,2 bis 80,3) unter EXTREME* ; Datenschnitt: 21.02.2022
±± Mediane Nachbeobachtungszeit: 69,7 Monate (Spanne: 61,7 bis 81,2) unter KEYTRUDA® plus Chemotherapie und 67,0 Monate (Spanne: 61,2 bis 80,3) für EXTREME (Datenschnitt: 21.02.2022)
$ Bewertet mittels verblindeter, unabhängiger und zentraler Beurteilung gemäß RECIST-v1.1-Kriterien.
¥ Der IQR ist ein Streuungsmaß der Statistik. Die beiden Werte geben an, in welchem Intervall sich die mittleren 50 % der Messwerte befinden.
Abkürzungen
5-FU: 5-Fluorouracil
AUC: area under the curve
CPS: combined positive score
CR: komplettes Ansprechen (complete response)
HR: Hazard Ratio
IQR: Interquartilsabstand (interquartile range)
KI: Konfidenzintervall
ORR: objektive Ansprechrate (overall response rate)
OS: Gesamtüberleben (overall survival)
PD-L1: Programmierter Zelltod-Ligand 1 (programmed death ligand 1)
PFS: progressionsfreies Überleben (progression free survival)
PR: partielles Ansprechen (partial response)
Q1W: wöchentlich
Q3W: alle drei Wochen
RECIST: Response Evaluation Criteria In Solid Tumors
TPS: tumor proportion score
Quellen
- Fachinformation KEYTRUDA®, Stand August 2024.
- Greil R et al. Treatment Sequencing in PD-L1-Positive Recurrent/Metastatic Head and Neck Squamous Cell Carcinoma: Exploratory Analysis of the Phase 3 KEYNOTE-048 Study. ESMO Immuno-Oncology Congress 2023. Poster #798.
- Burtness B et al. Pembrolizumab alone or with chemotherapy versus cetuximab with chemotherapy for recurrent or metastatic squamous cell carcinoma of the head and neck (KEYNOTE-048): A randomised, open-label, phase 3 study. The Lancet 2019; 394(10212):1915-1928.
- Tahara M et al. Pembrolizumab With or Without Chemotherapy For First-Line Treatment of Recurrent/Metastatic Head and Neck Squamous Cell Carcinoma: 5-year Results from KEYNOTE-048, ESMO 2022, oral presentation (Abstract #659MO).
DE-OHN-00260 10/24
Sie haben Fragen?
schnell – zuverlässig – kompetent
Unsere Ansprechpartner:innen
sind gerne für Sie da!
MSD Services
Vor der Verordnung eines Arzneimittels lesen Sie bitte die Fachinformation.
Fachinformationen
Gebrauchsinformationen
Sicherheitshinweise













