KEYNOTE-564: 5-Jahres-Follow-up unterstützt OS-Vorteil der adjuvanten KEYTRUDA®-Therapie
KEYNOTE-564: 5-Jahres-Follow-up unterstützt OS-Vorteil der adjuvanten KEYTRUDA®-Therapie
Mit fast 5 Jahren Nachbeobachtung liegen nun Daten zum Gesamtüberleben und krankheitsfreien Überleben der Phase-III-Studie KEYNOTE-564 vor. Die Ergebnisse zeigten eine anhaltend klinisch relevante Wirksamkeit von KEYTRUDA® in der adjuvanten Behandlung des RCC bei erhöhtem Rezidivrisiko, mit bekanntem Sicherheitsprofil.

Trotz Nephrektomie erleidet fast jeder zweite Patient mit Nierenzellkarzinom (RCC) innerhalb von fünf Jahren ein Rezidiv.1 Langzeit-Überlebensdaten können hier eine wichtige Rolle spielen. Seit Januar 2022 steht KEYTRUDA® zur Verfügung, als erste und bislang einzige zugelassene adjuvante Therapie für Patienten mit Nierenzellkarzinom, bei denen nach einer Nephrektomie oder nach Nephrektomie und Resektion metastasierter Läsionen ein erhöhtes Rezidivrisiko besteht.2 Grundlage war die Studie KEYNOTE-564, die bereits einen signifikanten Vorteil beim krankheitsfreien Überleben (DFS) und ein günstiges Sicherheitsprofil zeigte.2 Das aktuelle ASCO-Update 2025 unterstützt diese Ergebnisse nach fast fünf Jahren Nachbeobachtung mit anhaltendem Gesamtüberlebensvorteil (OS) und ohne neue Sicherheitssignale.3
Es zeigte sich unter KEYTRUDA® vs. Placebo in der Intent-to-treat (ITT)-Population (explorative Analyse) bei einer medianen Nachbeobachtungszeit von 69,5 Monaten (Spanne: 60,2 – 86,9)±:3
- 5-Jahres-Rate des DFS: 60,9 % unter KEYTRUDA® vs. 52,2 % unter Placebo
- 29,0 % Risikoreduktion mit einer HR von 0,71 (95-%-KI: 0,59 – 0,86)
- Ereignisse: 188/496 unter KEYTRUDA® vs. 241/498 unter Placebo
- Medianes DFS (95 %-KI): n. e. (n. e. – n. e.) unter KEYTRUDA® vs. 68,3 Monate (51,7 – n. e.) unter Placebo
OS-Daten der Studie KEYNOTE-564 (sekundärer Endpunkt)
Die explorative Analyse des sekundären Endpunkts OS (basierend auf Kaplan-Meier-Schätzungen) in der ITT-Population ergab nach einer medianen Nachbeobachtungszeit von 69,5 Monaten (Spanne 60,2 – 86,9)± 68 Todesereignisse unter Pembrolizumab (68/496) gegenüber 99 unter Placebo (99/498). Das mediane OS war in beiden Armen weiterhin nicht erreicht, womit der Überlebensvorteil zugunsten von KEYTRUDA® bestehen blieb.€, 3
![Die Abbildung zeigt Kaplan-Meier-Kurven zum Gesamtüberleben unter KEYTRUDA® vs. Placebo in der Studie KEYNOTE-564 (mediane Nachbeobachtungszeit 69,5 Monate [ITT-Population]). Grafik modifiziert von MSD nach Daten von Haas et al. 2025.3](https://www.msdconnect.de/wp-content/uploads/sites/100/2025/08/250807_MSD_Keytruda_KN-564.jpg?vip_files_acl=ODE2NjkyOTA3fDIwNjkzOA%3D%3D)
Abb. 1: Kaplan-Meier-Kurven zum Gesamtüberleben unter KEYTRUDA® vs. Placebo in der Studie KEYNOTE-564 (mediane Nachbeobachtungszeit 69,5 Monate [ITT-Population]). Grafik modifiziert von MSD nach Daten von Haas et al. 2025.3
Aktuelles Sicherheitsprofil
Auch über einen Zeitraum von fast fünf Jahren blieb KEYTRUDA® gut handhabbar: Therapiebedingte unerwünschte Ereignisse ≥ Grad 3 traten bei 18,6 % der Patienten auf (Placebo 1,2 %); therapiebedingte Todesfälle wurden in beiden Behandlungsarmen nicht beobachtet. Immunvermittelte unerwünschte Ereignisse und Infusionsreaktionen fanden sich in 36,5 % der Patienten unter KEYTRUDA® vs. 7,3 % unter Placebo. Seit über drei Jahren wurden damit keine neuen schwerwiegenden Nebenwirkungen registriert, sodass das Nutzen-Risiko-Profil auch nach fast fünf Jahren Follow-up unverändert günstig blieb.
Alle relevanten Daten zur Studie KEYNOTE-564 finden Sie hier in einer übersichtlichen Zusammenfassung:
Die zulassungsrelevante Phase-III-Studie KEYNOTE-564 ist eine multizentrische, randomisierte, doppelblinde, placebokontrollierte Studie.2 Das Ziel der Studie war es, die Wirksamkeit und Sicherheit von KEYTRUDA® als adjuvanter Behandlung bei Patienten mit RCC mit erhöhtem Rezidivrisiko nach Nephrektomie oder nach Nephrektomie und Resektion metastasierter Läsionen zu untersuchen.2
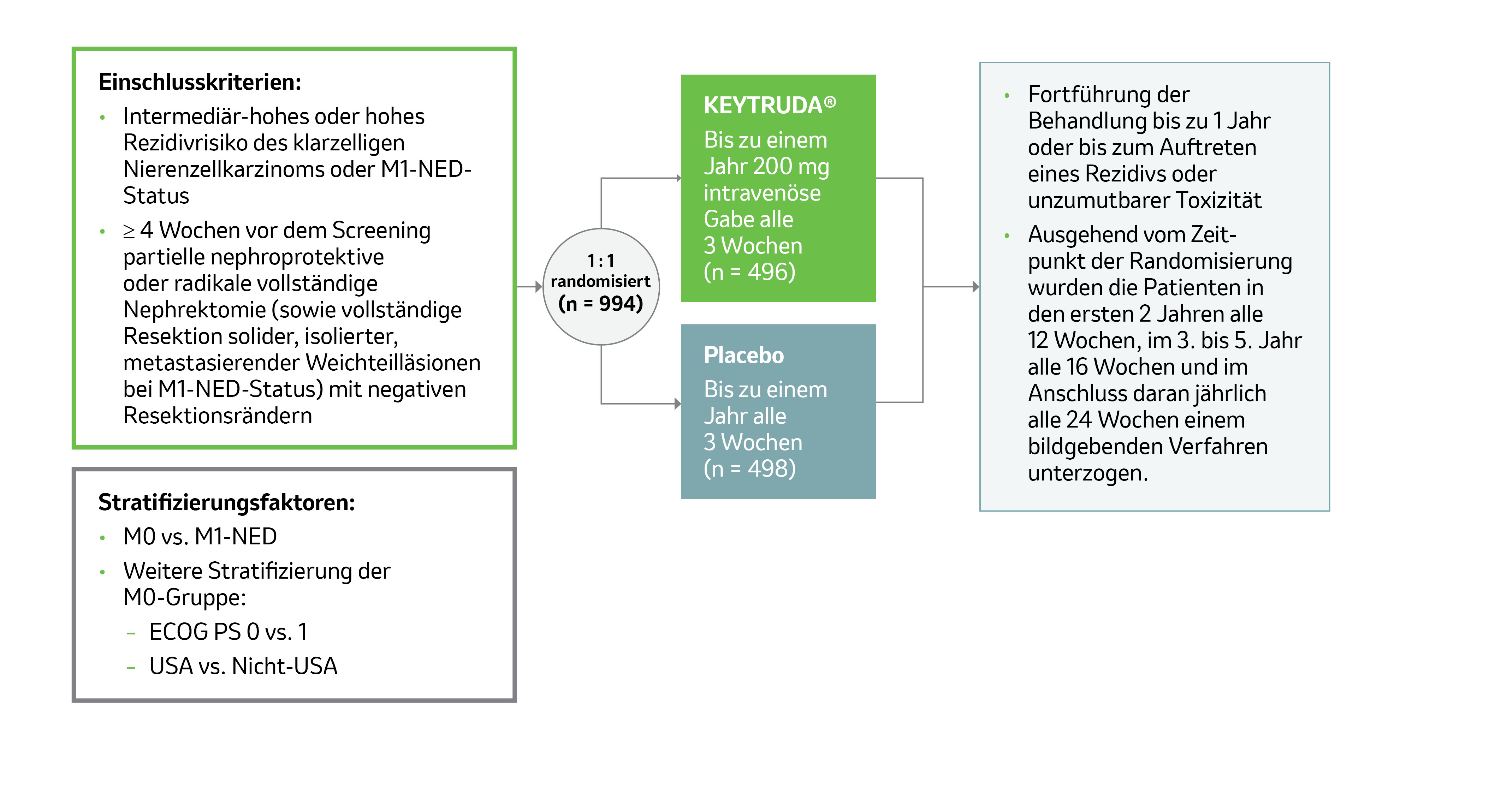
Abb. 2: Studiendesign der Phase-III-Studie KEYNOTE-564. Grafik modifiziert von MSD nach Daten der Fachinformation.2 NED = ohne Zeichen einer Erkrankung (no evidence of disease).
Die 994 Patienten mit RCC mit einer Klarzell-Komponente erhielten randomisiert (1 : 1) entweder KEYTRUDA® 200 mg alle drei Wochen (n = 496) oder Placebo (n = 498) bis zu einem Zeitraum von einem Jahr oder bis zum Auftreten eines Rezidivs oder unzumutbarer Toxizität.2
Die Randomisierung wurde nach Status der Metastasierung (M0; M1-NED) und innerhalb der M0-Gruppe weiter nach ECOG-Performance-Status (0; 1) und geografischer Region (USA; Nicht-USA) stratifiziert. Ausgehend vom Zeitpunkt der Randomisierung wurden die Patienten in den ersten zwei Jahren alle zwölf Wochen, im dritten bis fünften Jahr alle 16 Wochen und im Anschluss daran jährlich alle 24 Wochen einem bildgebenden Verfahren unterzogen.2
Haupteinschlusskriterien:2
- Patienten mit RCC mit intermediär-hohem oder hohem Rezidivrisiko (Einteilung siehe Tab. 1) oder mit M1-NED-Status.
- Patienten mussten sich einer partiellen nephroprotektiven oder radikalen vollständigen Nephrektomie (sowie einer vollständigen Resektion solider, isolierter, metastasierender Weichteilläsionen bei M1-NED-Patienten) mit negativen Resektionsrändern ≥ 4 Wochen vor Zeitpunkt des Screenings unterzogen haben.
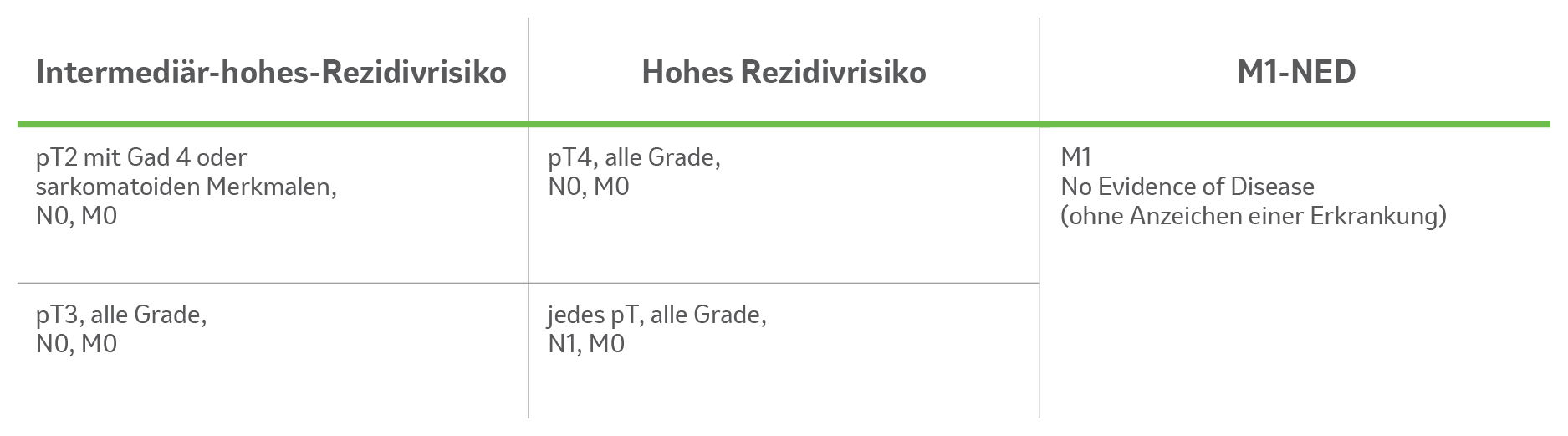
Tab. 1: Einteilung der Risikokategorien der Patienten mit RCC mit erhöhtem Rezidivrisiko zu Beginn der Phase-III-Studie KEYNOTE-564. Tabelle erstellt von MSD nach Daten der Fachinformation KEYTRUDA®.2
Hauptausschlusskriterien:2
- Eine aktive Autoimmunerkrankung
- Eine Erkrankung, die eine Immunsuppression erforderte
Primärer Wirksamkeitsendpunkt:2
- Krankheitsfreies Überleben$, beurteilt vom Prüfarzt
Wichtige sekundäre Endpunkte:2, 4
- Gesamtüberleben
- Analyse der gesundheitsbezogenen Lebensqualität auf Basis des FKSI-DRS Index Scores sowie des EORTC-QLQ-C30-Fragebogens
- Sicherheit
Patientencharakteristika zu Studienbeginn (ITT-Population££):
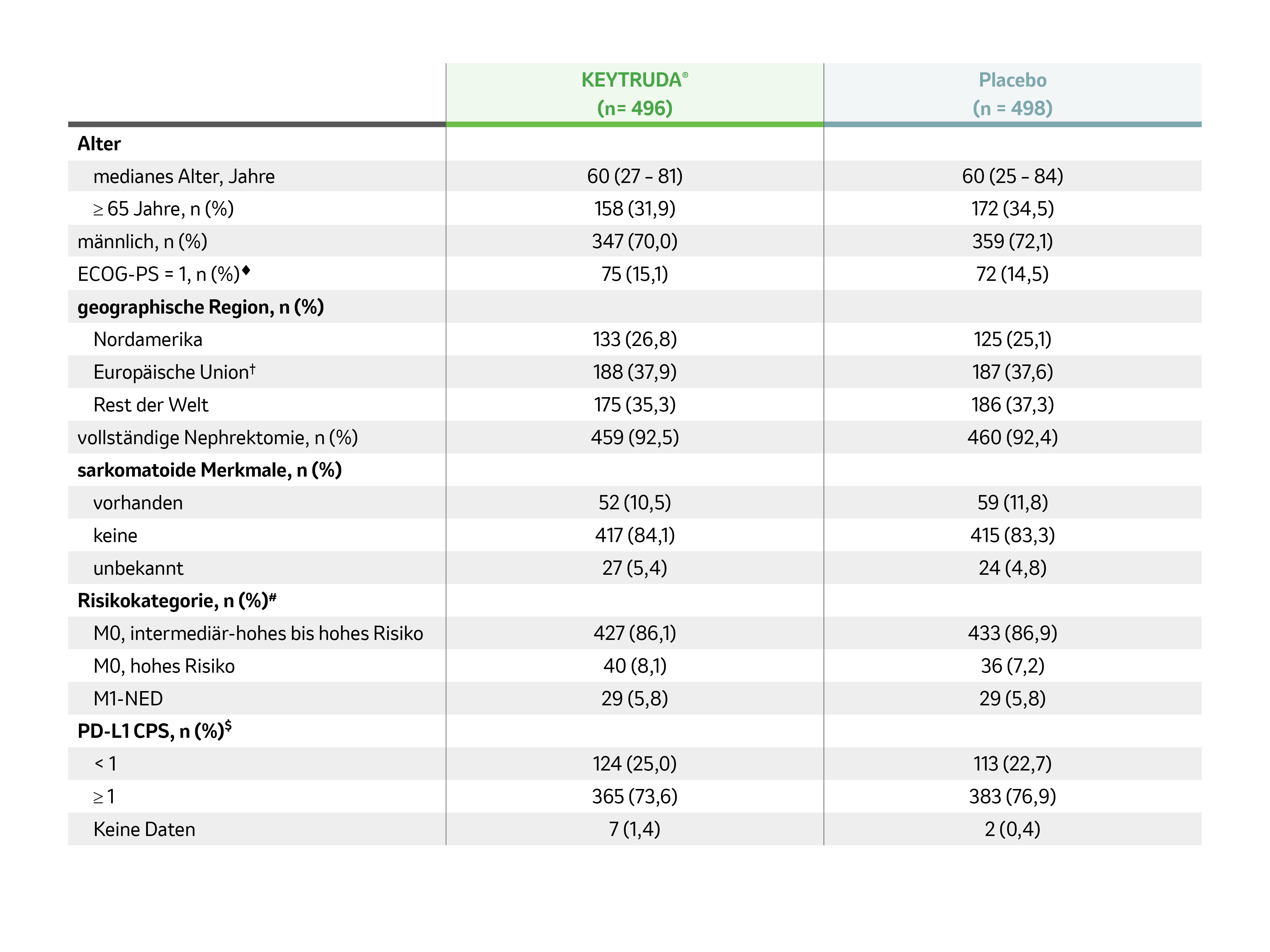
Tab. 2: Tabelle wichtiger Patientencharakteristika zu Beginn der Phase-III-Studie KEYNOTE-564. Tabelle erstellt von MSD nach Daten von Choueiri TK et al. 2021.4
Primärer Wirksamkeitsendpunkt krankheitsfreies Überleben
Statistisch signifikante Verbesserung des krankheitsfreien Überlebens unter KEYTRUDA® im Vergleich zu Placebo
Die zulassungsrelevante Analyse der Studie KEYNOTE-564 erfolgte nach einer medianen Nachbeobachtungszeit von 24,1 Monaten (von Randomisierung bis zum Datenschnitt am 14.12.2020, Spanne: 2,5 ‒ 41,5 Monate). In der ITT-Population££ zeigte sich ein DFS-Vorteil unter KEYTRUDA® gegenüber Placebo durch:4
- eine signifikante Verbesserung des DFS mit einer 32%igen Risikoreduktion für ein Rezidiv oder Tod (HR* = 0,68; 95 %-KI: 0,53 – 0,87; p = 0,002‡).4
- eine geschätzte 2-Jahres-DFS-Rate von 77,3 % (95 %-KI: 72,8 – 81,1) unter KEYTRUDA® vs. 68,1 % (95 %-KI: 63,5 – 72,2) unter Placebo.4
- das mediane DFS wurde in keinem der beiden Behandlungsarme erreicht.4
DFS basierend auf Kaplan-Meier-Schätzungen in der Studie KEYNOTE-564 (ITT-Population):
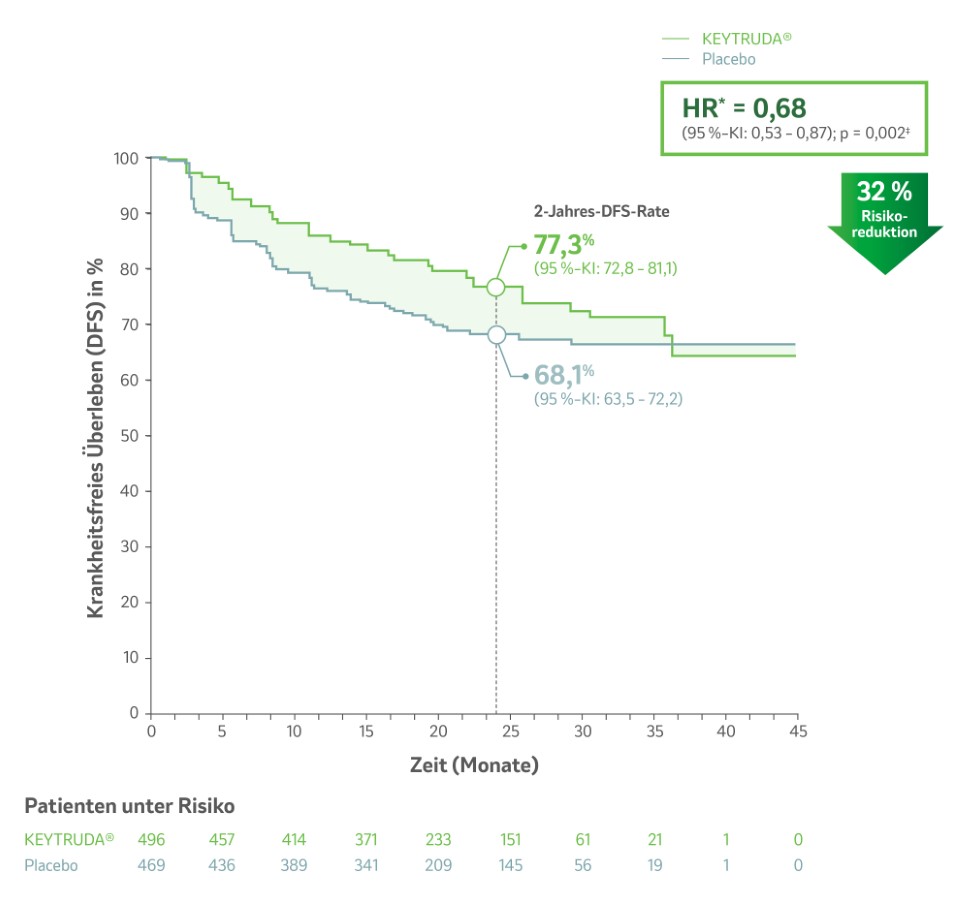
Abb. 3: Kaplan-Meier-Kurven zum krankheitsfreien Überleben unter KEYTRUDA® im Vergleich zu Placebo in der Studie KEYNOTE-564 (mediane Nachbeobachtungszeit 24,1 Monate**). Grafik modifiziert von MSD nach Daten von Choueiri TK et al. 2021.4
In der Studie KEYNOTE-564 traten keine neuen Sicherheitssignale auf. Das Sicherheitsprofil entsprach dem bekannten Sicherheitsprofil von KEYTRUDA®.5
Die Sicherheitsdaten der Studie KEYNOTE-564 nach einer medianen Nachbeobachtungszeit von 57,2 Monaten (von Randomisierung bis zum Datenschnitt am 15. September 2023, Spanne: 47,9–74,5) beziehen sich auf die As-treated-Population§ (n = 488).5
Die mediane Behandlungsdauer betrug 11,1 Monate (Spanne: 0,03‒14,3 Monate) mit KEYTRUDA® und ebenfalls 11,1 Monate (Spanne: 0,03‒15,4 Monate) unter Placebo.5
Da bereits alle Teilnehmer die Studienbehandlung vor 2 Jahren abgeschlossen oder abgebrochen hatten, blieb das Sicherheitsprofil in der präspezifizierten Interimsanalyse (IA3) konsistent mit den Daten früherer Auswertungen.5
Unerwünschte Ereignisse (UE) und Nebenwirkungen traten mit folgenden Häufigkeiten auf:5
- UE vom Grad 3–5: 32,0 % (KEYTRUDA®-Arm) vs. 17,7 % (Placebo-Arm).
- Immunvermittelte UEs jeglichen Grades: 36,5 % (KEYTRUDA®-Arm) vs. 7,3 % (Placebo-Arm).
- Immunvermittelte UEs vom Grad 3‒4: 9,4 % (KEYTRUDA®-Arm) vs. 0,6 % (Placebo-Arm).
- Es ereignete sich kein Todesfall aufgrund eines immunvermittelten UEs. Es gab keine Todesfälle, die auf die Behandlung mit KEYTRUDA® zurückgeführt werden konnten.
- In der As-treated-Population§ kam es aufgrund von UEs bei 21,1 % der Patienten unter KEYTRUDA® vs. 2,2 % unter Placebo zu einem Therapieabbruch.
- In keinem der beiden Behandlungsgruppen wurden UEs vom Grad 5 beobachtet.
Unerwünschte Ereignisse, die in einer der beiden Gruppen (As-Treated-Population§) bei ≥ 5 % der Patienten auftraten (Datenschnitt: 15. September 2023):5
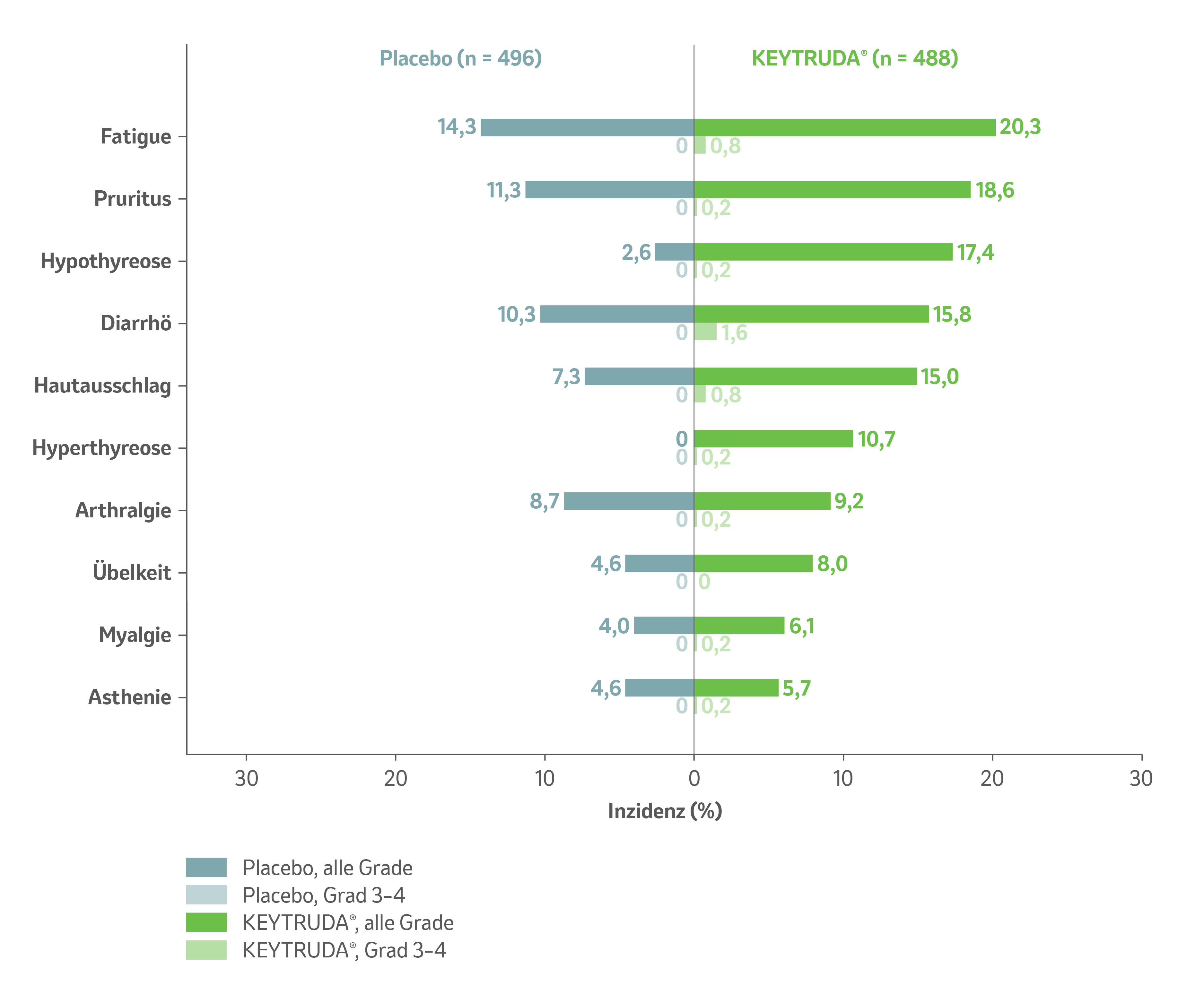
Abb. 6: Unerwünschte Ereignisse mit Inzidenz ≥ 5 % unter KEYTRUDA® im Vergleich zu Placebo in der in der As-treated-Population§ der Studie KEYNOTE-564 (mediane Nachbeobachtungszeit 57,2 Monaten). Grafik modifiziert von MSD nach Daten von Choueiri et al., 2024.5
Fazit
KEYTRUDA® ist weiterhin die erste und bislang einzige zugelassene adjuvante Therapie beim RCC mit erhöhtem Rezidivrisiko. Die 5-Jahresdaten zu DFS und OS zeigten eine anhaltende Verbesserung unter KEYTRUDA® vs. Placebo und waren in allen wichtigen Subgruppen konsistent, einschließlich präspezifizierter Risikokategorien und sarkomatoider Merkmale – bei einem gut charakterisierten Sicherheitsprofil.
Weitere Informationen:
Studienseite KEYNOTE-564
OS-Daten inklusive Subgruppenanalyse
Daten zur gesundheitsbezogenen Lebensqualität (HRQoL)
Anmerkungen
± Datenschnitt: 25.09.2024.
€ Der wichtigste sekundäre OS-Endpunkt wurde bei IA3 erreicht und danach nicht mehr formal statistisch getestet.
‡ 2-seitiger p-Wert, basierend auf dem stratifizierten Log-Rank-Test.
* HR basierend auf dem stratifizierten Cox-Proportional-Hazard-Modell.
** Mediane Zeit von Randomisierung bis zum Datenschnitt.
$ Das DFS war definiert als die Zeit von Randomisierung bis zum ersten dokumentierten und vom Prüfarzt festgestellten Auftreten des ersten Rezidivs des Nierenzellkarzinoms (lokal oder Fernmetastasen) oder bis zum Tod aus jeglichem Grund, je nachdem, was als erstes auftrat.
† Zur Zeit der Studie gehörte Großbritannien zur EU.
# Einteilung der Risikokategorien siehe Tab. 1.; 5 Patienten in der M0 intermediär-hohen Risikogruppe hatten T2 (mit Grad ≤ 3), N0, M0 oder T1 (Nierentumor von nur ≤ 7 cm maximaler Größe), N0, M0. Dies waren Protokollverletzungen. $ Der programmierter Zelltod-Ligand 1 (PD-L1) Combined Positive Score (CPS) ist definiert als Anteil der PD-L1-positiven Tumor- und Immunzellen (Lymphozyten und Makrophagen) im Verhältnis zu allen Tumorzellen, multipliziert mit 100.
££ ITT-Population = alle Patienten, die randomisiert wurden.
Die Summe der Prozentangaben ergeben aufgrund von Rundungen möglicherweise keine 100 %.
§As-treated-Population umfasst alle Patienten, die mind. eine Dosis der zugewiesenen Therapie mit KEYTRUDA® oder Placebo erhalten haben.
Abkürzungen
CPS: combined positive score
DFS: krankheitsfreies Überleben (disease-free survival)
ECOG PS: Eastern Co-operative Oncology Group Performance Status
EORTC QLQ: European Organisation for Research and Treatment of Cancer Quality of Life Questionnaire
FKSI-DRS: Functional Assessment of Cancer Therapy – Kidney Symptom Index
HR: hazard ratio
HRQoL: Gesundheitsbezogene Lebensqualität
IA: Interimsanalyse
ITT: Intent-to-treat
KI: Konfidenzintervall
n. e.: nicht erreicht
NED: ohne Zeichen einer Erkrankung (no evidence of disease)
OS: Gesamtüberleben (overall survival)
PD-L1: programmierter Zelltod-Ligand 1 (programmed cell death ligand 1)
RCC: Nierenzellkarzinom (renal cell carcinoma)
UE: unerwünschtes Ereignis
vs.: versus
Quellen
- Haas NB et al. Variation in recurrence rate and overall survival (OS) outcomes by disease stage and incremental impact of time to recurrence on OS in localized renal cell carcinoma (RCC). JCO 2022; 40(16_suppl):4543.
- Fachinformation KEYTRUDA®, Stand Juni 2025 (B).
- Haas NB et al. Five-year follow-up results from the phase 3 KEYNOTE-564 study of adjuvant pembrolizumab (pembro) for the treatment of clear cell renal cell carcinoma (ccRCC).: ASCO Annual Meeting; Rapied Oral Abstract Session #4514; 2025.
- Choueiri TK et al. Adjuvant Pembrolizumab after Nephrectomy in Renal-Cell Carcinoma. N Engl J Med 2021; 385(8):683–94.
- Choueiri TK et al. Overall Survival with Adjuvant Pembrolizumab in Renal-Cell Carcinoma (inkl. Supplement). N Engl J Med 2024; 390(15):1359–71.
DE-KEY-00944 08/25
Sie haben Fragen?
schnell – zuverlässig – kompetent
Unsere Ansprechpartner:innen
sind gerne für Sie da!
MSD Services
Vor der Verordnung eines Arzneimittels lesen Sie bitte die Fachinformation.
Fachinformationen
Gebrauchsinformationen
Sicherheitshinweise