AGO-Empfehlung 2025 eTNBC: KEYTRUDA®-basierte Therapie mit der höchsten Bewertung „++“ als Therapiestandard bestätigt
AGO-Empfehlung 2025 eTNBC: KEYTRUDA®-basierte Therapie mit der höchsten Bewertung „++“ als Therapiestandard bestätigt
Die Arbeitsgemeinschaft Gynäkologische Onkologie e.V. (AGO) hat in den neuen Empfehlungen von 2025 die KEYTRUDA®-basierte Therapie für geeignete Patienten mit frühen TNBC als Standard bestätigt und den höchsten Empfehlungsgrad „++“ ausgesprochen.

Die KEYTRUDA®-basierte Therapie† für geeignete Patienten mit frühem TNBC wurde von der Arbeitsgemeinschaft Gynäkologische Onkologie e. V. (AGO), Kommission Mamma, als Standard bestätigt und mit „++“ bewertet. Eine solche „++“ Bewertung ist der höchste Grad der Empfehlung, den die AGO ausspricht.1
Die KEYTRUDA®-basierte Therapie† beim lokal fortgeschrittenen oder frühen TNBC mit hohem Rezidivrisiko (≥ cT2 oder pN+) in der neoadjuvanten Therapie, gefolgt von adjuvanter KEYTRUDA®-Monotherapie† wird mit einem „++“ für beide Therapiephasen empfohlen.1,2 Dies entspricht einer Komplettierung der Therapie auf insgesamt ein Jahr.
Die AGO empfiehlt bereits seit 2022 die Komplettierung der adjuvanten KEYTRUDA®-Monotherapie† auf insgesamt ein Jahr (mit 17 Zyklen) durch eine „++“-Bewertung, sofern eine neoadjuvante Therapie† mit dem Immuncheckpoint-Inhibitor in Kombination mit einer Chemotherapie begonnen wurde.1,3–5 Mit der Empfehlung von 2025 ist das KEYTRUDA®-basierte Therapieschema† beim frühen TNBC inklusive neoadjuvanter Behandlung für bestimmte Patienten mit frühem TNBC laut AGO mit „++“ uneingeschränkt empfohlen.1
Hier sehen Sie den entsprechenden Abschnitt der AGO-Empfehlung:
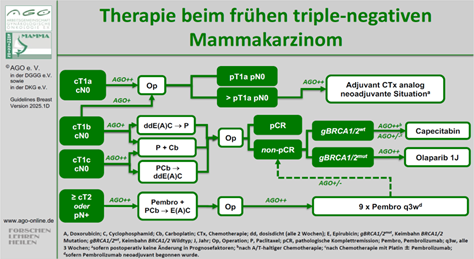
Abb. 1: Ausschnitt aus dem Therapiealgorithmus der AGO‑Empfehlungen zum frühen triple-negativen Mammakarzinom (TNBC). Abbildung modifiziert nach Empfehlungen der AGO, Kommission Mamma, 2025.1y8
Die Spanne der AGO-Bewertungen reicht von „- -“ (Diese therapeutische Intervention ist für die Patienten von klarem Nachteil und sollte in jedem Fall vermieden oder unterlassen werden) bis hin zur höchsten Bewertung „++“ (Diese therapeutische Intervention ist für die Patienten von großem Vorteil, sie kann uneingeschränkt empfohlen und sollte durchgeführt werden).1
Hier werden die vollständigen Empfehlungen der AGO veröffentlicht (Abschnitt „Therapiealgorithmen“).
Weitere Informationen zur AGO finden Sie unter www.ago-online.de.
Disclaimer
Die weiterführenden Links verweisen auf unabhängige Informationsquellen und stellen nicht notwendigerweise die Meinung von MSD dar. MSD übernimmt keine Gewähr oder Verantwortung für deren Richtigkeit, Vollständigkeit und Aktualität. Die Beiträge drücken die alleinigen Ansichten der jeweiligen Autoren aus.
NCCN-Leitlinie
Auch die Brustkrebs-Leitlinie des NCCN (National Comprehensive Cancer Network) wurde Anfang des Jahres 2025 aktualisiert.
Für Patienten mit frühem TNBC in den Stadien II–III* wird KEYTRUDA® (Pembrolizumab) plus Paclitaxel und Carboplatin neoadjuvant, gefolgt von KEYTRUDA® plus Cyclophosphamid und Doxorubicin oder Epirubicin neoadjuvant, gefolgt von KEYTRUDA®-Monotherapie adjuvant, nun mit Kategorie 1§ empfohlen.6
KEYTRUDA® (Pembrolizumab) ist in Kombination mit Chemotherapie zur neoadjuvanten und anschließend nach Operation als Monotherapie zur adjuvanten Behandlung des lokal fortgeschrittenen oder frühen triple-negativen Mammakarzinoms mit hohem Rezidivrisiko bei Erwachsenen angezeigt.2
Erfahren Sie mehr zu den Daten der Studie KEYNOTE-522 und der KEYTRUDA®-basierten Therapie† im neoadjuvanten und adjuvanten Setting bei bestimmten Patienten mit frühem triple-negativem Mammakarzinom (TNBC) vs. Placebo-Regime.
AGO-Empfehlung zum fortgeschrittenen Mammakarzinom
Die AGO bestätigte außerdem in den Empfehlungen 2025 den Therapiestandard zur Behandlung des fortgeschrittenen TNBC mit PD-L1-Positivität (Combined Positive Score [CPS] ≥ 10) mit KEYTRUDA® in Kombination mit Chemotherapie mit einer „++“-Empfehlung.1
KEYTRUDA® (Pembrolizumab) ist in Kombination mit Chemotherapie zur Behandlung des lokal rezidivierenden nicht resezierbaren oder metastasierenden triple-negativen Mammakarzinoms mit PD L1 exprimierenden Tumoren (Combined Positive Score [CPS] ≥ 10) bei Erwachsenen, die keine vorherige Chemotherapie zur Behandlung der metastasierenden Erkrankung erhalten haben, angezeigt.2
Erfahren Sie mehr zur zugehörigen Zulassungsstudie KEYNOTE-355 und zur KEYTRUDA®-basierten Therapie† bei bestimmten Patienten mit fortgeschrittenem triple-negativem Mammakarzinom (TNBC) in der Erstlinie vs. Placebo-Regime.
Anmerkungen
† KEYTRUDA®-Regime: vier Zyklen neoadjuvante Therapie mit KEYTRUDA® (200 mg) i.v. Q3W an Tag 1 der Zyklen 1–4 des Behandlungsregimes in Kombination mit Paclitaxel (80 mg/m2 i.v., Q1W an den Tagen 1, 8 und 15 der dreiwöchigen Zyklen 1–4 des Behandlungsregimes) und Carboplatin (AUC 1,5 mg/ml/min i.v., Q1W an den Tagen 1, 8 und 15 oder AUC 5 mg/ml/min i.v., Q3W an Tag 1 der dreiwöchigen Zyklen des Behandlungsregimes), gefolgt von vier weiteren Zyklen neoadjuvanter Therapie mit KEYTRUDA® (200 mg) i.v. Q3W an Tag 1 der dreiwöchigen Zyklen 5–8 in Kombination mit Cyclophosphamid (600 mg/m2 i.v., Q3W an Tag 1 der dreiwöchigen Zyklen 5–8) und Doxorubicin (60 mg/m2 i.v., Q3W an Tag 1 der dreiwöchigen Zyklen 5–8) oder Epirubicin (90 mg/m2 i.v., Q3W an Tag 1 der dreiwöchigen Zyklen 5–8). Im Anschluss an die Operation wurden neun Zyklen adjuvante Monotherapie mit KEYTRUDA® (200 mg) i.v., Q3W an Tag 1 der dreiwöchigen Zyklen des Behandlungsregimes verabreicht.
* Tumorstadien II-III (Staging des NCCN nach AJCC cancer staging manual):
- Stadium IIA: T0N1M0; T1N1M0; T2N0M0
- Stadium IIB: T2N1M0; T3N0M0
- Stadium IIIA: T0N2M0; T1N2M0; T2N2M0; T3N1M0; T3N2M0
- Stadium IIIB: T4N0M0; T4N1M0; T4N2M0
- Stadium IIIC: T (alle) N3M0
§ Kategorie 1 der NCCN-Kategorien der Evidenz und des Konsenses: Auf der Grundlage hochwertiger Evidenz (≥1 randomisierte Phase-III-Studie oder hochwertige, robuste Meta-Analysen) besteht ein einheitlicher NCCN-Konsens (≥85% Unterstützung durch das Gremium), dass die Intervention angemessen ist.
Abkürzungen
A: Doxorubicin
AGO: Arbeitsgemeinschaft Gynäkologische Onkologie e. V.
AJCC: American Joint Committee on Cancer der American Cancer Society
BRCA: Breast Cancer Susceptibility Gene
C: Cyclophosphamid
Cb: Carboplatin
CPS: combined positive score
CTx: Chemotherapie
dd: dosisdicht (alle 2 Wochen)
E: Epirubicin EFS: ereignisfreie Überleben
eTNBC: frühes triple-negatives Mammakarzinom
gBR-CA1/2mut: Keimbahn BRCA1/2 Mutation
gBRCA1/2wt: Keimbahn BRCA1/2 Wildtyp
J: Jahr
NCCN: National Comprehensive Cancer Network
non-pCR: keine pathologische Komplettremission
Op: OperationOS: Gesamtüberleben
P: Paclitaxel
pCR: pathologische Komplettremissionsrate
PD-L1: programmierter Zelltod-Ligand 1 (programmed cell death ligand 1)
Pembro: Pembrolizumab
Q3W: alle 3 Wochen
Q6W: alle 6 Wochen
pos: positiv
TNBC: triple-negatives Mammakarzinom (triple-negative breast cancer)
Quellen
- AGO Kommission Mamma. Diagnostik und Therapie früher und fortgeschrittener Mammakarzinome. Empfehlungen 2025.
- Fachinformation KEYTRUDA®, Stand Januar 2025.
- Arbeitsgemeinschaft Gynäkologische Onkologie (AGO) Kommission Mamma. Diagnostik und Therapie früher und fortgeschrittener Mammakarzinome. Empfehlung 2022.
- Arbeitsgemeinschaft Gynäkologische Onkologie (AGO) Kommission Mamma. Diagnostik und Therapie früher und fortgeschrittener Mammakarzinome. Empfehlung 2023.
- Arbeitsgemeinschaft Gynäkologische Onkologie (AGO) Kommission Mamma. Diagnostik und Therapie früher und fortgeschrittener Mammakarzinome. Empfehlung 2024.
- Clinical Practice Guidelines in Oncology. NCCN Guidelines. Version 3.2025. Invasive Breast Cancer.
DE-OBR-00029 02/25
Sie haben Fragen?
schnell – zuverlässig – kompetent
Unsere Ansprechpartner:innen
sind gerne für Sie da!
MSD Services
Vor der Verordnung eines Arzneimittels lesen Sie bitte die Fachinformation.
Fachinformationen
Gebrauchsinformationen
Sicherheitshinweise