Studie: KEYNOTE-A39
Studie KEYNOTE-A39: Zulassung von KEYTRUDA® + Enfortumab Vedotin in 1L beim nicht resezierbaren oder metastasierenden Urothelkarzinom
Zulassungsstudie von KEYTRUDA® (Pembrolizumab) + Enfortumab Vedotin zur Erstlinienbehandlung des nicht resezierbaren oder metastasierenden Urothelkarzinoms.

Ziel der Studie
In der zulassungsrelevanten Studie KEYNOTE-A39 wurden die Wirksamkeit und Sicherheit von KEYTRUDA® (Pembrolizumab) in Kombination mit Enfortumab Vedotin (EV) im Vergleich zu platinhaltiger Chemotherapie bei Patienten mit nicht resezierbarem lokal fortgeschrittenem oder metastasierendem Urothelkarzinom in Erstlinie untersucht.1, 2
KEYTRUDA® ist in Kombination mit Enfortumab Vedotin zur Erstlinienbehandlung des nicht resezierbaren oder metastasierenden Urothelkarzinoms bei Erwachsenen angezeigt.2
Wichtige Ergebnisse auf einen Blick
Zulassungsrelevant waren die Ergebnisse der Studie KEYNOTE-A39 mit einer medianen Nachbeobachtungszeit von 17,2 Monaten (Datenschnitt: 08.08.2023). In der Analyse wurden in der Intent-to-treat (ITT)-Population unter KEYTRUDA® + EV (n = 442) gegenüber platinhaltiger Chemotherapie† (n = 444) folgende Ergebnisse erfasst:1
Weitere detaillierte und relevante Daten zur Wirksamkeit und Sicherheit aus der Studie KEYNOTE-A39 finden Sie weiter unten übersichtlich zusammengefasst.
Die Studie KEYNOTE-A39 ist eine offene, multizentrische, randomisierte, aktiv-kontrollierte Studie von KEYTRUDA® + EV im Vergleich zu platinhaltiger Chemotherapie†. Es waren 886 Patienten mit nicht resezierbarem lokal fortgeschrittenem oder metastasierendem Urothelkarzinom eingeschlossen.1
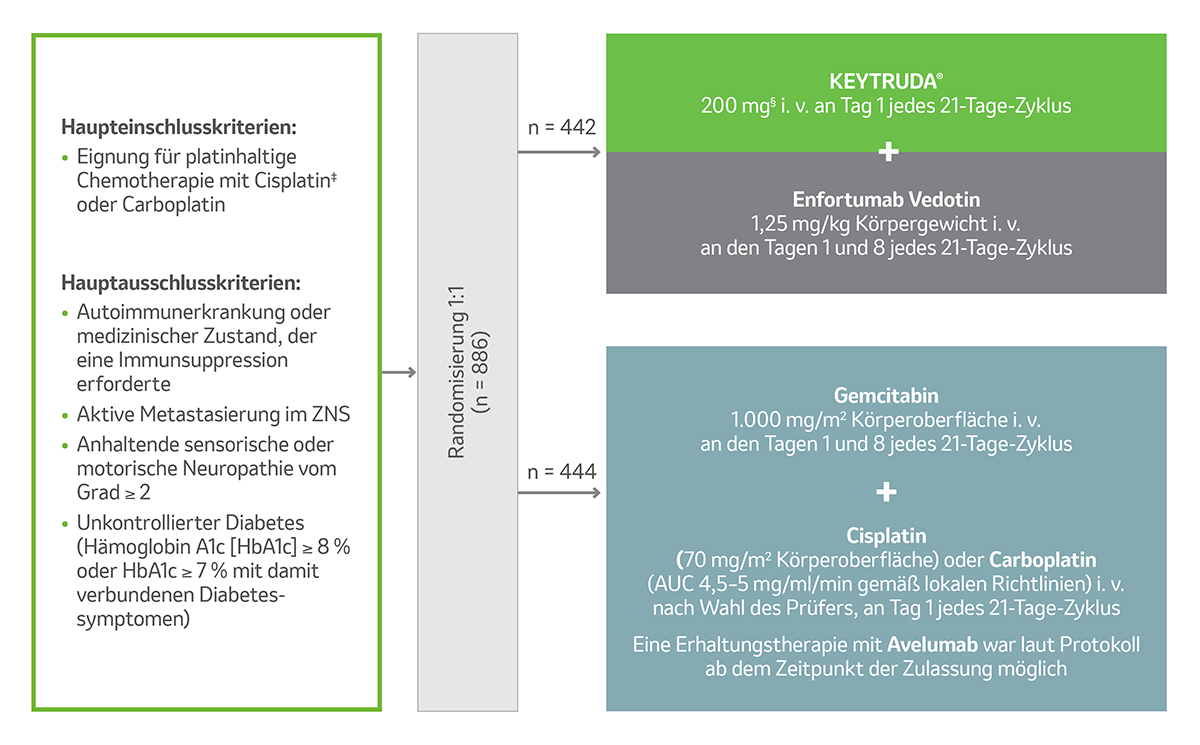
Abb. 1: Studiendesign der KEYNOTE-A39 in den beiden Behandlungsarmen. Grafik modifiziert von MSD nach Daten von Powles T et al 2024.1
‡ Patienten wurden als Cisplatin-ungeeignet betrachtet, wenn sie mindestens eines der folgenden Kriterien erfüllten: glomeruläre Filtrationsrate ≥ 30 und < 60 ml/min, ECOG PS 2, Hörverlust Grad ≥ 2 oder Herzinsuffizienz NYHA-Klasse III.
§ i. v.-Infusion über 30 Minuten. Bei Verabreichung am selben Tag wurde KEYTRUDA® nach Enfortumab Vedotin verabreicht.
Die Patienten wurden 1:1 randomisiert und einem der folgenden Behandlungsarme zugeteilt:1
- KEYTRUDA® 200 mg intravenös (i. v.) über 30 Minuten an Tag 1 jedes 21-Tage-Zyklus + EV 1,25 mg/kg i. v. an Tag 1 und 8 jedes 21-Tage-Zyklus
- Gemcitabin 1.000 mg/m2 i. v. an den Tagen 1 und 8 und nach Maßgabe des Prüfarztes entweder Cisplatin 70 mg/m2 oder Carboplatin (AUC 4,5 oder 5 mg/ml/min gemäß lokalen Richtlinien) an Tag 1 jedes 21-Tage-Zyklus. Eine Erhaltungstherapie mit Avelumab war laut Protokoll ab dem Zeitpunkt der Zulassung möglich.
Die Behandlung mit KEYTRUDA® und Enfortumab Vedotin wurde bis zum Fortschreiten der Krebserkrankung*, bis zum Auftreten unzumutbarer Toxizität, oder bei KEYTRUDA® bis zu einem Maximum von 35 Zyklen (bis zu ca. 2 Jahren) fortgeführt.1
Die Beurteilung des Tumorstatus erfolgte 18 Monate lang alle 9 Wochen und danach alle 12 Wochen.1
Haupteinschlusskriterien:1
- Erwachsene Patienten mit nicht resezierbarem lokal fortgeschrittenem oder metastasierendem Urothelkarzinom
- Eignung für platinhaltige Chemotherapie mit Cisplatin‡ oder Carboplatin
Hauptausschlusskriterien:1
- Autoimmunerkrankung oder medizinischer Zustand, der eine Immunsuppression erforderte
- Aktive Metastasierung im Zentralnervensystem
- Anhaltende sensorische oder motorische Neuropathie vom Grad ≥ 2
- Unkontrollierter Diabetes (Hämoglobin A1c [HbA1c] ≥ 8 % oder HbA1c ≥ 7 % mit damit verbundenen Diabetessymptomen)
Stratifizierungsfaktoren:1
- Cisplatin-Eignung (geeignet oder nicht geeignet)
- PD-L1-Expression (hoch: CPS ≥ 10 oder niedrig: CPS < 10)
- Lebermetastasen (vorhanden oder nicht vorhanden)
Primäre Wirksamkeitsendpunkte:1
- Gesamtüberleben (OS)
- Progressionsfreies Überleben (PFS); bewertet mittels einer verblindeten, unabhängigen und zentralen Beurteilung (BICR) gemäß RECIST-v1.1-Kriterien
Wichtige sekundäre Wirksamkeitsendpunkte:1
- Objektive Ansprechrate (ORR); bewertet mittels einer verblindeten, unabhängigen und zentralen Beurteilung (BICR) gemäß RECIST-v1.1-Kriterien
- Dauer des Ansprechens (DOR); bewertet mittels einer verblindeten, unabhängigen und zentralen Beurteilung (BICR) gemäß RECIST-v1.1-Kriterien
- Zeit bis zur Schmerzprogression
Baseline Charakteristika
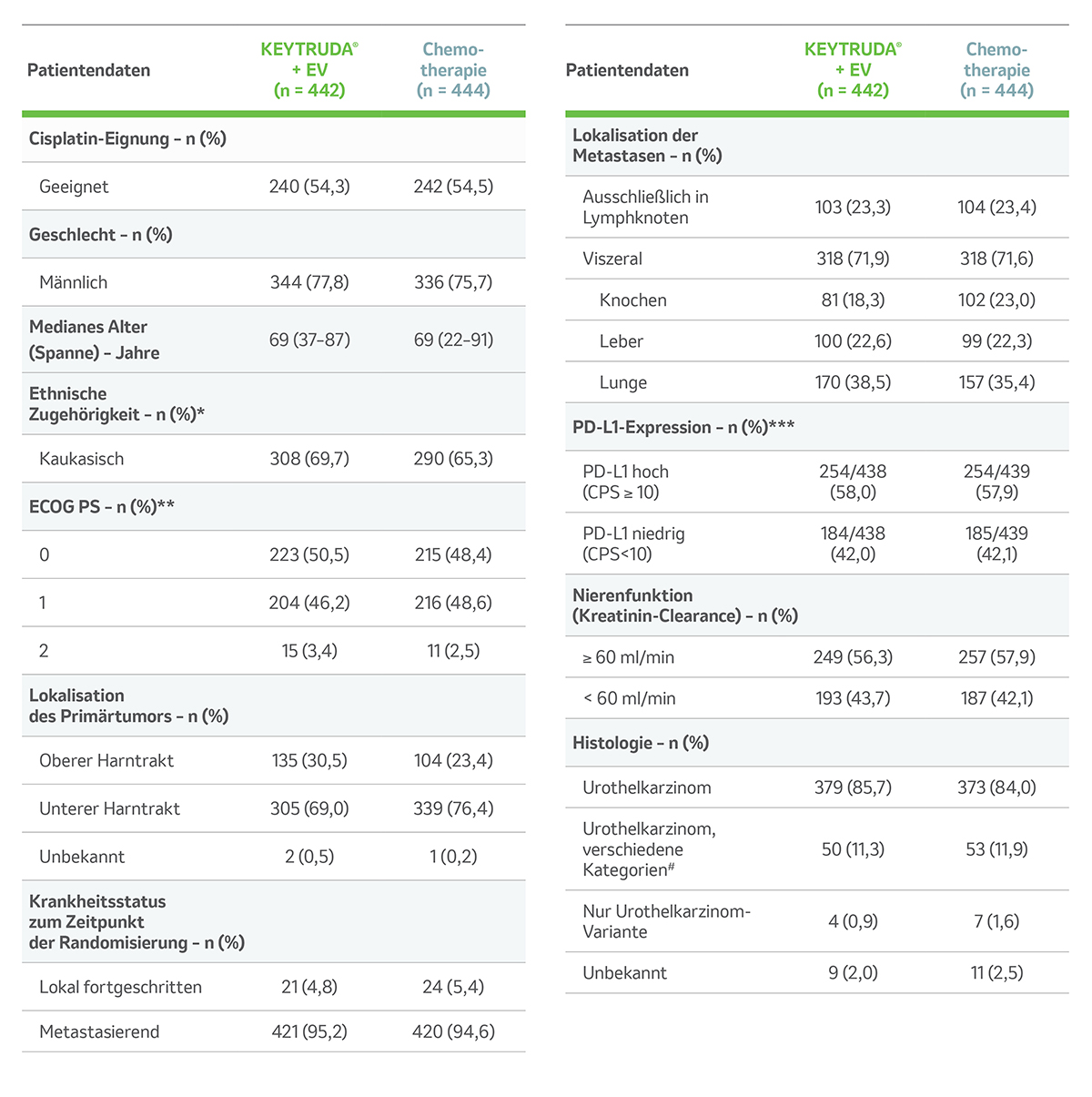
Tab. 1: Tab.1: Tabelle mit den Baseline-Charakteristika zu Beginn der Phase-III-Studie KEYNOTE-A39. Tabelle modifiziert von MSD nach Daten von Powles T et al. 2024.1
* Zugehörigkeit wurde vom Patienten angegeben; ** Bewertung des Eastern Cooperative Oncology Group (ECOG) Performance-Status rangiert von 0 bis 5, wobei ein höherer Wert auf eine stärkere Einschränkung hinweist; *** Die Expression des Programmed death ligand 1 (PD-L1) wurde mit dem PD-L1 IHC 22C3 pharmDx Assays (Agilent Technologies) bestimmt. Der combined positive score (CPS) wurde definiert als die Menge von PD-L1-gefärbten Zellen (Tumor- und Immunzellen, Lymphozyten und Makrophagen), die durch die Anzahl aller Zellen geteilt und mit 100 multipliziert wurde; **** Diese Kategorie inkludiert histologische Kategorien wie plattenepithelial, glandulär und mikropapillär.
Primärer Wirksamkeitsendpunkt: Progressionsfreies Überleben (PFS)£
Überlegenes PFS unter KEYTRUDA® + EV vs. platinhaltiger Chemotherapie†
In der zulassungsrelevanten Analyse wurde nach einer medianen Nachbeobachtungszeit von 17,2 Monaten (Datenschnitt: 08.08.2023) für den primären Wirksamkeitsendpunkt PFS unter KEYTRUDA® + EV (n = 442) gegenüber platinhaltiger Chemotherapie† (n = 444) Folgendes beobachtet:1
- eine 55%-ige statistisch signifikante Reduktion des Risikos für Progression oder Tod (PFS, Hazard Ratio [HR#] = 0,45; 95 %– Konfidenzintervall [KI]: 0,38–0,54; p < 0,001±).
- nahezu eine Verdopplung des medianen PFS unter KEYTRUDA® + EV (12,5 Monate; 95 %-KI: 10,4–16,6) vs. platinhaltiger Chemotherapie† (6,3 Monate; 95 %-KI: 6,2–6,5).
- Beobachtete Ereignisse: 223/442 unter KEYTRUDA® + EV vs. 307/444 unter Chemotherapie
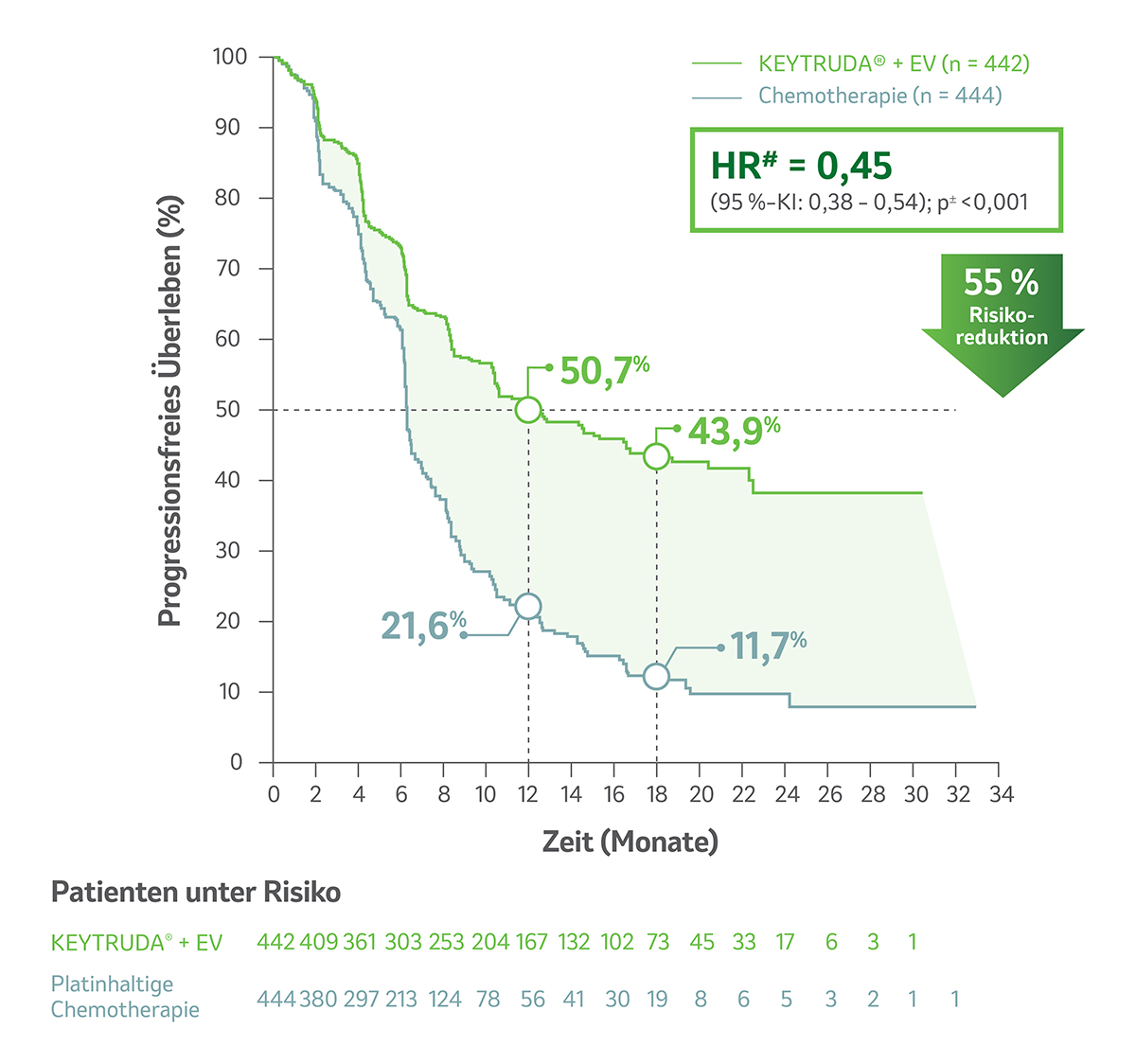
Abb. 2: Kaplan-Meier-Kurven zum PFS unter KEYTRUDA® + EV vs. platinhaltiger Chemotherapie† in der Studie KEYNOTE-A39 nach einer medianen Nachbeobachtungszeit von 17,2 Monaten für die ITT-Population. Grafik modifiziert von MSD nach Daten von Powles T et al. 2024.1
# Basierend auf dem Cox-Proportional-Hazard-Regressionsmodell; ± Zweiseitiger p-Wert basierend auf stratifiziertem Log-Rank-Test
Die Ergebnisse zur Wirksamkeit zum PFS waren über alle präspezifizierten Subgruppen wie z. B. Metastasen in der Leber, Cisplatin-Eignung und PD-L1-Tumorexpression vergleichbar.1
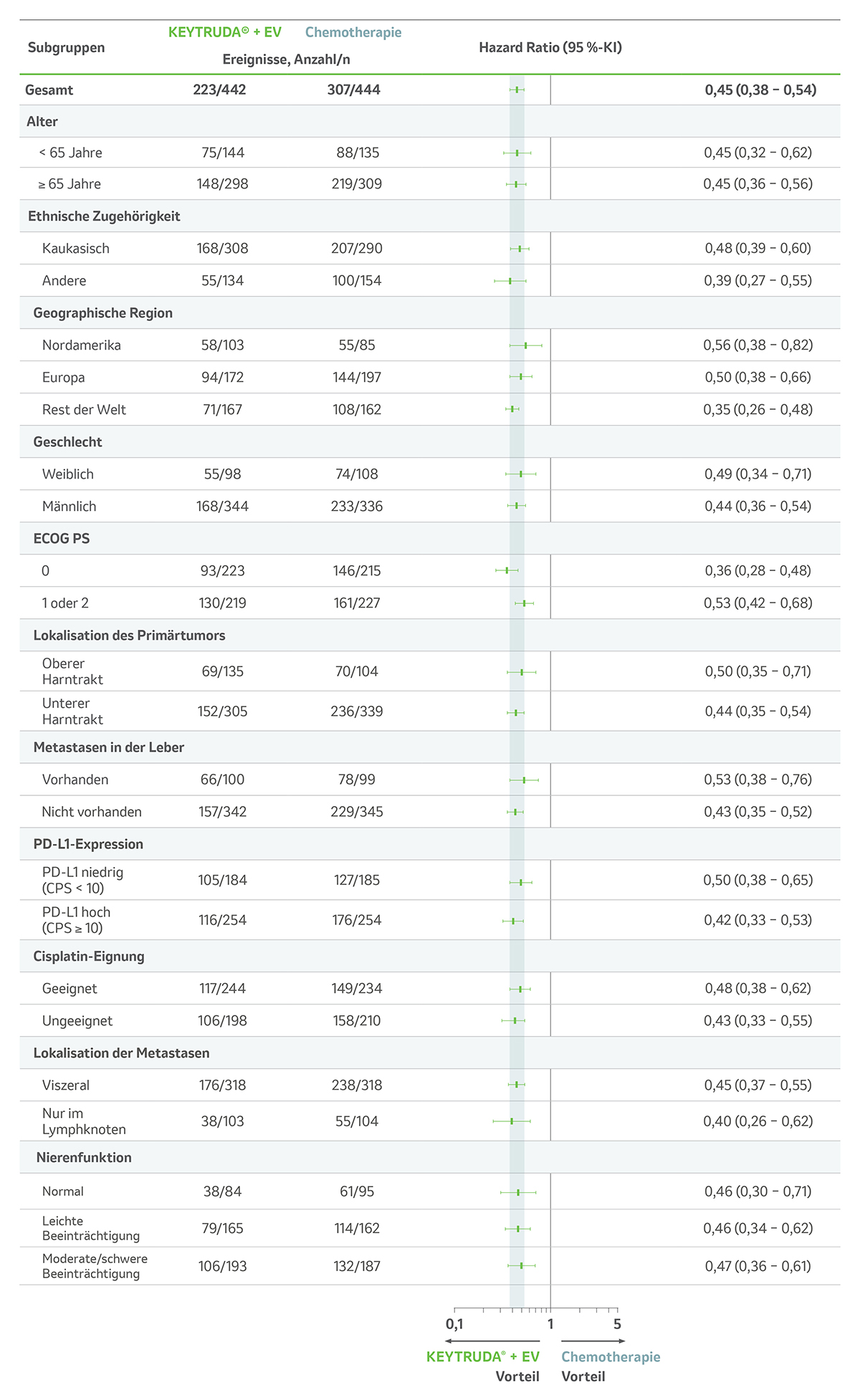
Abb. 3: Explorative Analyse zum PFS in präspezifizierten Subgruppen unter KEYTRUDA® + EV vs. platinhaltiger Chemotherapie† in der Studie KEYNOTE-A39 nach einer medianen Nachbeobachtungszeit von 17,2 Monaten. Grafik modifiziert von MSD nach Daten von Powles T et al. 2024.1
Primärer Wirksamkeitsendpunkt: Gesamtüberleben (OS)
Halbierung des Sterberisikos unter KEYTRUDA® + EV vs. platinhaltiger Chemotherapie†
Nach einer medianen Nachbeobachtungszeit von 17,2 Monaten (Datenschnitt: 08.08.2023) zeigte sich für den primären Wirksamkeitsendpunkt OS unter KEYTRUDA® + EV (n = 442) gegenüber platinhaltiger Chemotherapie† (n = 444):1
- eine Reduktion des Sterberisikos um 53 % (HR# = 0,47; 95 %-KI: 0,38–0,58; p < 0,001±) unter KEYTRUDA® + EV gegenüber platinhaltiger Chemotherapie†.
- Das mediane OS betrug 31,5 Monate (95 %-KI: 25,4–n.e.) unter KEYTRUDA® + EV im Vergleich zu 16,1 Monaten (95 %-KI: 13,9–18,3) unter platinhaltiger Chemotherapie†.
- Beobachtete Ereignisse: 133/442 unter KEYTRUDA® + EV vs. 226/444 unter Chemotherapie.
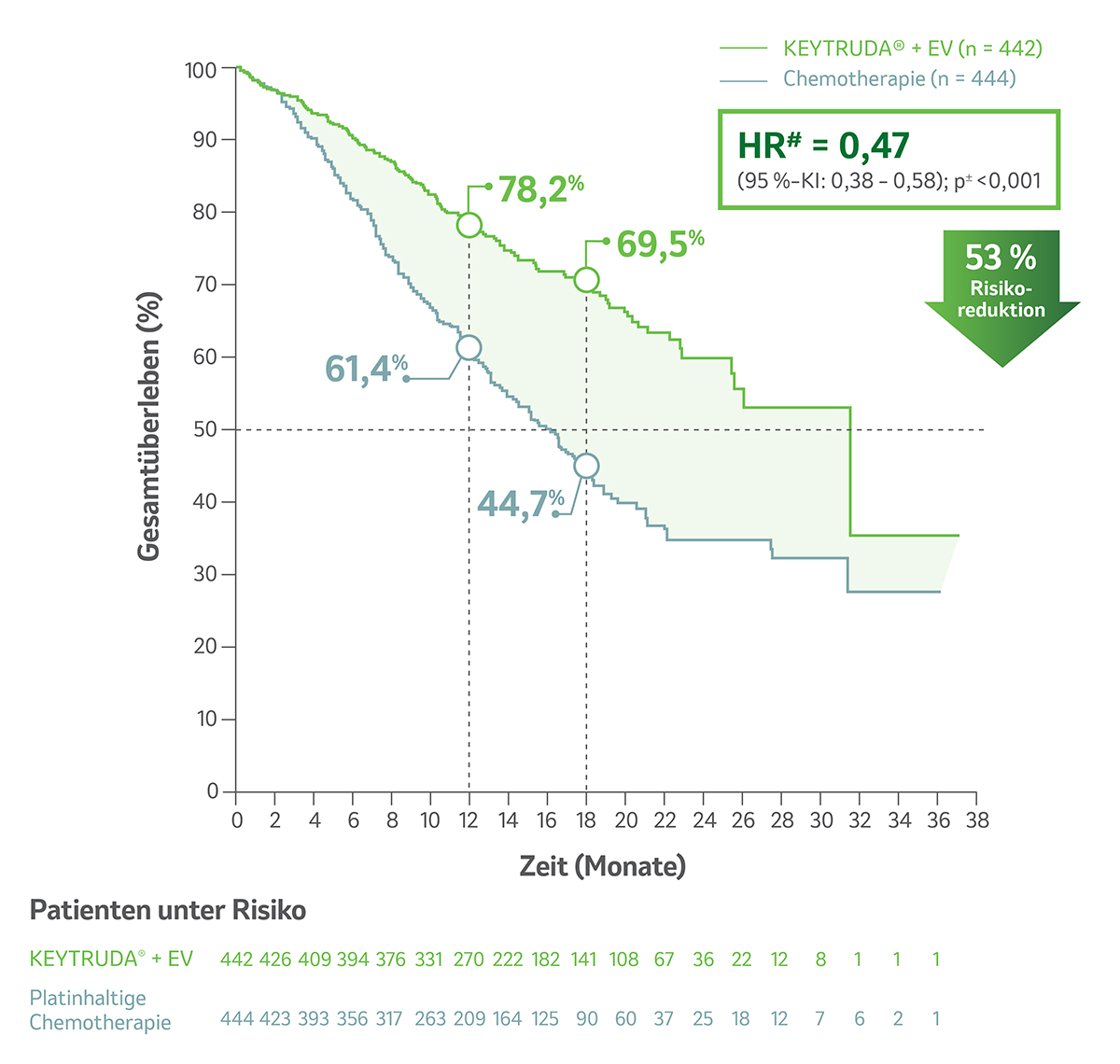
Abb. 4: Kaplan-Meier-Kurven zum OS unter KEYTRUDA® + EV vs. platinhaltiger Chemotherapie† in der Studie KEYNOTE-A39 nach einer medianen Nachbeobachtungszeit von 17,2 Monaten für die ITT-Population. Grafik modifiziert von MSD nach Daten von Powles T et al. 2024.1
# Basierend auf dem Cox-Proportional-Hazard-Regressionsmodell; ± Zweiseitiger p-Wert basierend auf stratifiziertem Log-Rank-Test
Auch die Ergebnisse zur Wirksamkeit zum OS waren über alle präspezifizierten Subgruppen wie z. B. Metastasen in der Leber, Cisplatin-Eignung und PD-L1-Tumorexpression vergleichbar.1
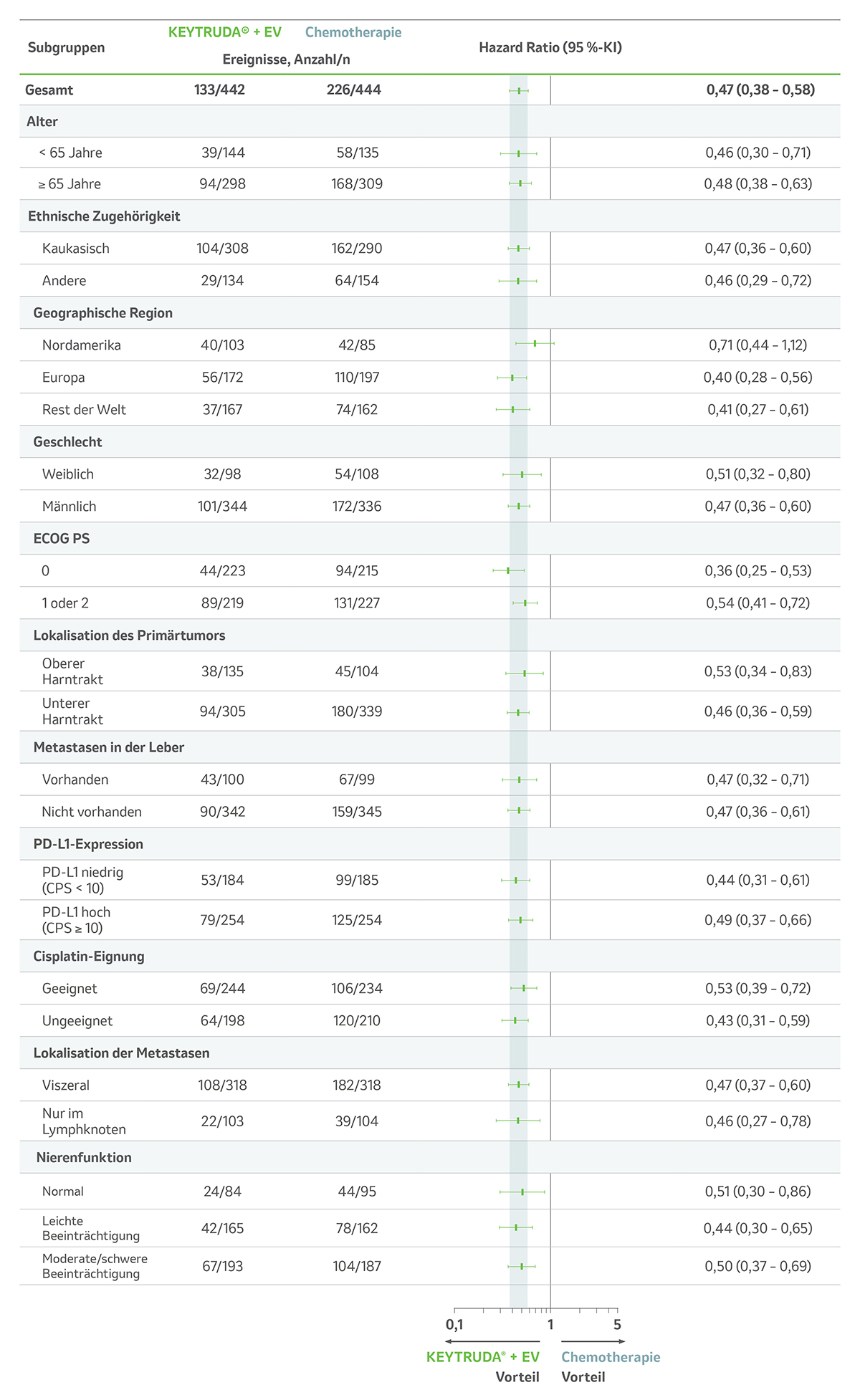
Abb. 5: Explorative Analyse zum OS in präspezifizierten Subgruppen unter KEYTRUDA® + EV vs. platinhaltiger Chemotherapie† in der Studie KEYNOTE-A39 nach einer medianen Nachbeobachtungszeit von 17,2 Monaten. Grafik modifiziert von MSD nach Daten von Powles T et al. 2024.1
Sekundärer Wirksamkeitsendpunkt: Objektive Ansprechrate (ORR)£, $
In der zulassungsrelevanten Analyse der Studie KEYNOTE-A39 wurde nach einer medianen Nachbeobachtungszeit von 17,2 Monaten (Datenschnitt: 08.08.2023) in der ITT-Population folgende Ansprechrate (ORR) erreicht:1
- eine ORR von 67,7 % (95 %-KI: 63,1 %–72,1 %) unter KEYTRUDA® + EV (n = 437) im Vergleich zu 44,4 % (95 %-KI: 39,7 %–49,2 %) unter platinhaltiger Chemotherapie† (n = 441).
- Ein vollständiges Ansprechen (CR) wurde bei 29,1 % der Patienten unter KEYTRUDA® + EV vs. 12,5 % unter platinhaltiger Chemotherapie† beobachtet.1
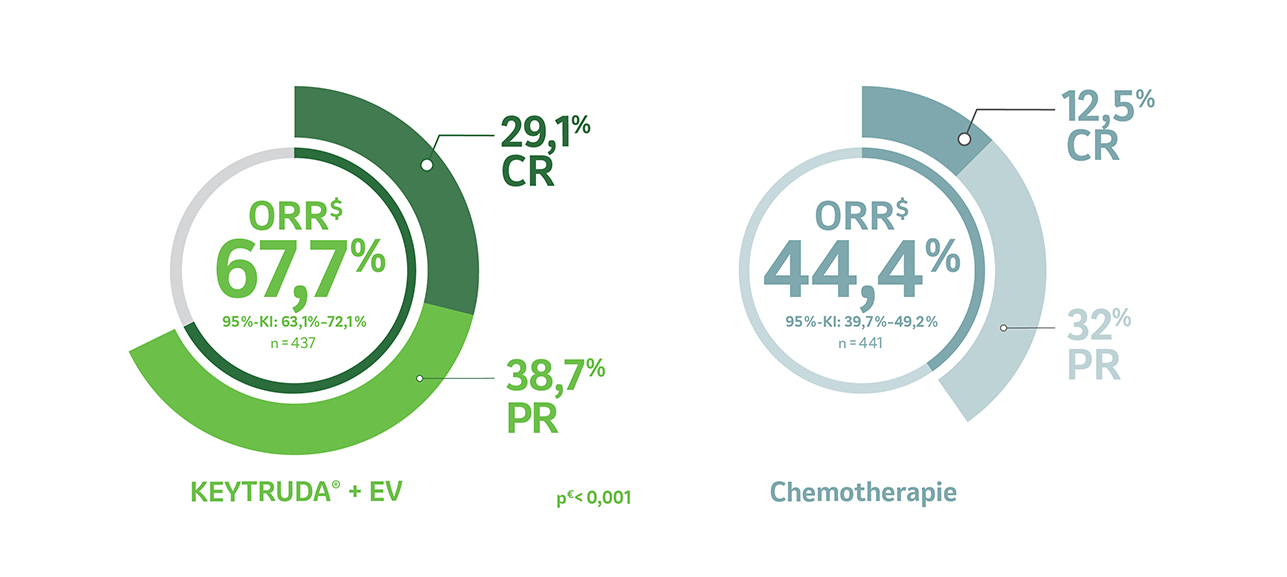
Abb. 6: Abbildung zur ORR$ (sekundärer Endpunkt) unter KEYTRUDA® + EV vs. platinhaltiger Chemotherapie† in der Studie KEYNOTE-A39 nach einer medianen Nachbeobachtungszeit von 17,2 Monaten für die ITT-Population. Grafik modifiziert von MSD nach Daten von Powles T et al. 2024.1
$ Umfasst nur Patienten mit messbarer Erkrankung zu Beginn der Studie, bei denen als bestes Ansprechen eine Komplettremission oder partielle Remission bestätigt wurde; € Zweiseitiger p-Wert basierend auf Cochran-Mantel-Haenszel-Test
In der explorativen Analyse waren die erfassten Ergebnisse zur ORR über alle präspezifizierten Subgruppen wie z. B. Metastasen in der Leber, Cisplatin-Eignung und PD-L1-Tumorexpression vergleichbar.1
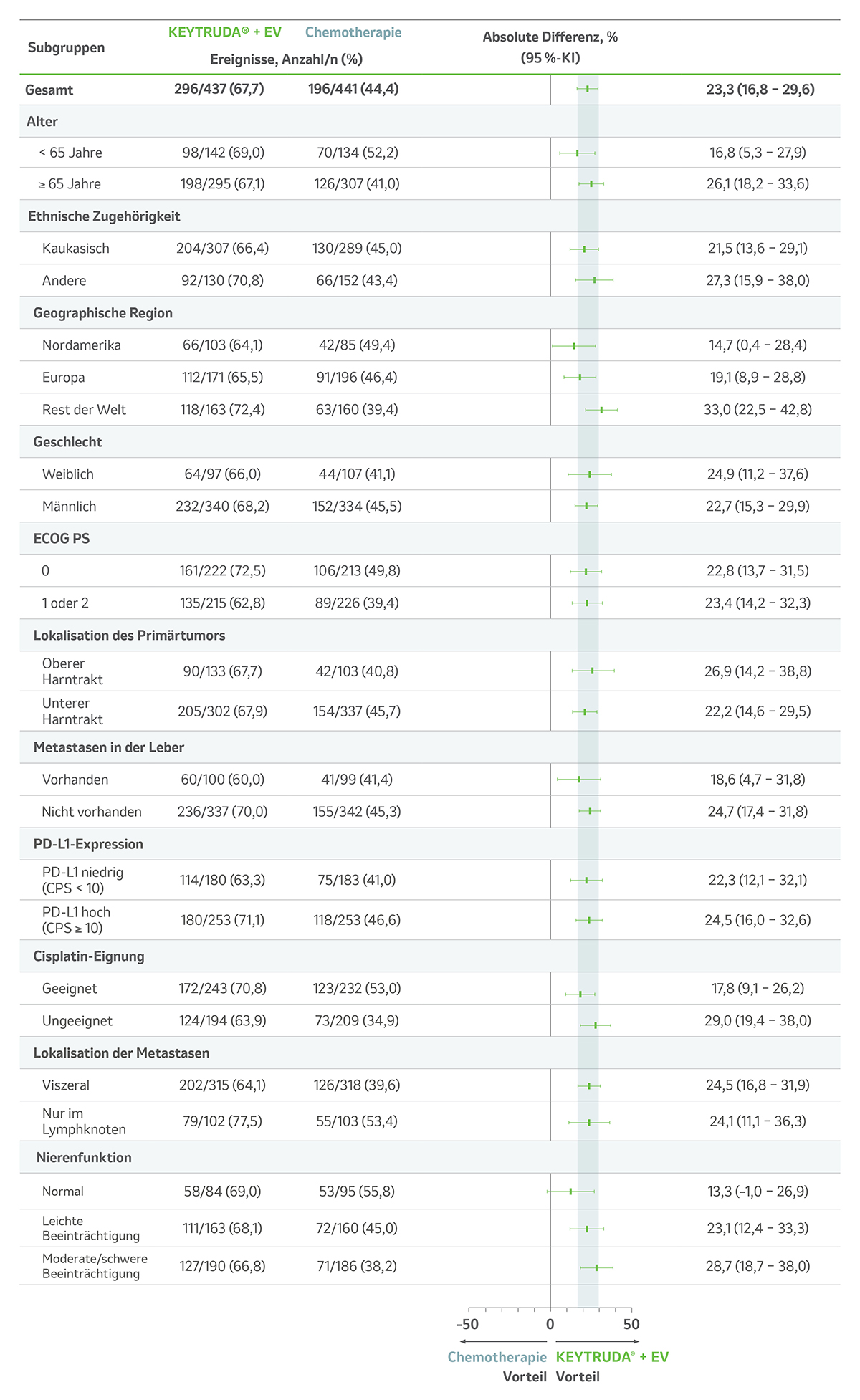
Abb. 7: Subgruppenanalysen zur ORR (sekundärer Endpunkt) unter KEYTRUDA® + EV vs. platinhaltiger Chemotherapie† in der Studie KEYNOTE-A39 nach einer medianen Nachbeobachtungszeit von 17,2 Monaten. Grafik modifiziert von MSD nach Daten von van der Powles T et al. 2024.1
Sekundärer Wirksamkeitsendpunkt: Dauer des Ansprechens (DOR)£
Die Analyse für die DOR in der KEYNOTE-A39 zeigte nach einer medianen Nachbeobachtungszeit von 17,2 Monaten in der ITT-Population:1
- Unter KEYTRUDA® + EV (n = 437) wurde die mediane DOR noch nicht erreicht (20,2–n.e.). Unter platinbasierter Chemotherapie† (n = 441) betrug sie 7,0 Monate (6,2–10,2).
- Basierend auf Kaplan-Meier-Schätzungen sprachen nach ≥ 18 Monaten 59,6 % der Patienten unter KEYTRUDA® + EV weiterhin auf die Therapie an. Unter platinbasierter Chemotherapie† waren es 19,3 %.

Tab. 2: Tabelle mit Angaben zur DOR (sekundärer Endpunkt) unter KEYTRUDA® + EV vs. platinhaltiger Chemotherapie† in der Studie KEYNOTE-A39 nach einer medianen Nachbeobachtungszeit von 17,2 Monaten für die ITT-Population. Grafik modifiziert von MSD nach Daten von Powles T et al. 2024.1
¥ Basierend auf Kaplan-Meier-Schätzung
Die Nebenwirkungen ähnelten im Allgemeinen denen bei Patienten, die KEYTRUDA® oder EV als Monotherapie erhielten
In der zulassungsrelevanten Studie KEYNOTE-A39 wurde die Sicherheit in der As-treated-Population◊ nach einer medianen Behandlungsdauer von 9,4 Monaten (Spanne: 0,3–31,9 Monate) unter KEYTRUDA® + EV über median 12 Zyklen (Spanne: 1–46) und 4,1 Monate (Spanne: 0,0–0,7) über median 6 Zyklen (Spanne: 1–6) unter platinhaltiger Chemotherapie† untersucht. Die mediane Behandlungsdauer mit KEYTRUDA® betrug dabei 8,5 Monate (Spanne: 0,3–28,5) über median 11 Zyklen (Spanne: 1–35).1
Unerwünschte Ereignisse (UE)¶ und Nebenwirkungen wurden mit folgender Häufigkeit unter KEYTRUDA® + EV (n = 440) vs. platinhaltiger Chemotherapie† (n = 433) beobachtet:1
- Nebenwirkungen vom Grad ≥ 3 traten bei 55,9 % der Patienten unter KEYTRUDA® + EV gegenüber 69,5 % unter platinbasierter Chemotherapie† auf.
- Häufigste Nebenwirkungen von Grad ≥ 3: makulopapulöser Ausschlag (7,7 %), Hyperglykämie (5,0 %) und Neutropenie (4,8 %) im KEYTRUDA® + EV-Arm.
- UEs vom Grad ≥ 3 von besonderem Interesse, die mit KEYTRUDA® assoziiert wurden:
- Schwere Hautreaktionen (11,8 % der Patienten), Pneumonitis (3,6 %) und Hepatitis (1,8 %).
- Behandlungsbedingte UEs mit Todesfolge (Multiorganversagen, immunvermittelte Lungenerkrankung, Diarrhö und Asthenie) traten bei 4 Patienten (< 1,0 %) im KEYTRUDA® + EV-Arm auf.
Zu einem Behandlungsabbruch mit KEYTRUDA® führten behandlungsbedingte UEs bei 21,4 % der Patienten.
Zu einer Dosierunterbrechung von KEYTRUDA® aufgrund von behandlungsbedingten UEs kam es bei 49,5 % der Patienten.
UEs, die bei ≥ 20 % der Patienten in einer der Behandlungsgruppen der As-treated-Population◊ auftraten:1
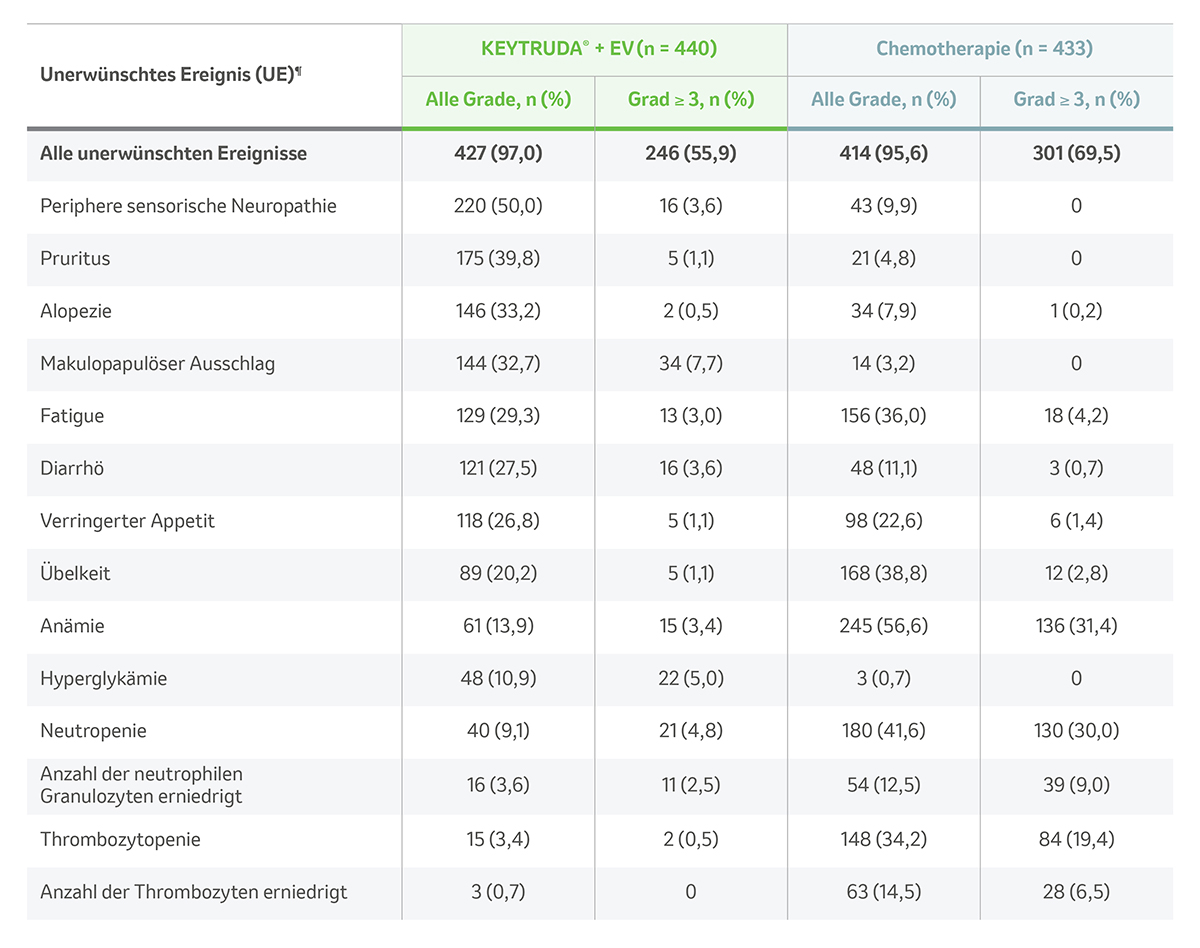
Tab. 3: UEs nach Graden, die in der As-treated-Population der Studie KEYNOTE-A39 auftraten. Abbildung modifiziert von MSD nach Daten von Powles T et al. 2024.1
¶ Aufgeführt sind behandlungsbedingte UEs, die bei mindestens 20 % der Patienten in einem der Behandlungsarme aufgetreten sind, und behandlungsbedingte UEs von Grad 3 oder höher, die bei mindestens 5 % der Patienten in einem der Behandlungsarme aufgetreten sind. Behandlungsbedingte UEs sind solche mit begründeter Annahme des teilnehmenden Arztes, dass sie durch die Studienmedikation verursacht wurden.
Die UEs unter KEYTRUDA® + EV ähnelten im Allgemeinen denen bei Patienten, die KEYTRUDA® oder EV als Monotherapie erhielten. Die Häufigkeit von makulopapulösem Ausschlag betrug 36 % jeglichen Schweregrades (davon 10 % Grad 3–4) und war somit höher als unter KEYTRUDA®-Monotherapie.2
Anmerkungen
† Gemcitabin 1.000 mg/m2 i. v. an den Tagen 1 und 8 und nach Maßgabe des Prüfarztes entweder Cisplatin 70 mg/m2 oder Carboplatin (AUC 4,5 oder 5 mg/ml/min gemäß lokalen Richtlinien) an Tag 1 jedes 21-Tage-Zyklus. Eine Erhaltungstherapie mit Avelumab war laut Protokoll ab dem Zeitpunkt der Zulassung möglich.
£ Bewertet mittels einer verblindeten, unabhängigen und zentralen Beurteilung („Blinded Independent central Review“ [BICR]) gemäß RECIST-v1.1-Kriterien.
$ Umfasst nur Patienten mit messbarer Erkrankung zu Studienbeginn und basiert auf Patienten, bei denen als bestes Ansprechen eine Komplettremission oder partielle Remission bestätigt wurde.
# Basierend auf dem Cox-Proportional-Hazard-Regressionsmodell.
± Zweiseitiger p-Wert basierend auf stratifiziertem Log-Rank-Test.
◊ Die As-treated-Population inkludierte alle Patienten, die mindestens eine Dosis der Studienmedikation erhalten haben.
& Aufgeführt sind behandlungsbedingte UEs, die bei mindestens 20 % der Patienten in einem der Behandlungsarme aufgetreten sind, und behandlungsbedingte UEs von Grad 3 oder höher, die bei mindestens 5 % der Patienten in einem der Behandlungsarme aufgetreten sind. Behandlungsbedingte UEs sind solche mit begründeter Annahme des teilnehmenden Arztes, dass sie durch die Studienmedikation verursacht wurden.
‡ Patienten wurden als Cisplatin-ungeeignet betrachtet, wenn sie mindestens eines der folgenden Kriterien erfüllten: glomeruläre Filtrationsrate ≥ 30 und < 60 ml/min, ECOG PS 2, Hörverlust Grad ≥ 2 oder Herzinsuffizienz NYHA-Klasse III.
§ i. v.-Infusion über 30 Minuten. Bei Verabreichung am selben Tag wurde KEYTRUDA® nach Enfortumab Vedotin verabreicht.
* Zugehörigkeit wurde vom Patienten angegeben.
** Bewertung des Eastern Cooperative Oncology Group (ECOG) Performance-Status rangiert von 0 bis 5, wobei ein höherer Wert auf eine stärkere Einschränkung hinweist.
*** Die Expression des Programmed death ligand 1 (PD-L1) wurde mit dem PD-L1 IHC 22C3 pharmDx Assays (Agilent Technologies) bestimmt. Der combined positive score (CPS) wurde definiert als die Menge von PD-L1-gefärbten Zellen (Tumor- und Immunzellen, Lymphozyten und Makrophagen), die durch die Anzahl aller Zellen geteilt und mit 100 multipliziert wurde.
**** Diese Kategorie inkludiert histologische Kategorien wie plattenepithelial, glandulär und mikropapillär.
€ p-Wert basierend auf Cochran-Mantel-Haenszel-Test.
¥ Basierend auf Kaplan-Meier-Schätzung.
Abkürzungen
AUC: area under the curve
BICR: verblindete, unabhängige und zentrale Beurteilung (Blinded Independent Central Review)
CPS: combined positive score
CR: vollständiges Ansprechen (complete response)
DOR: Dauer des Ansprechens (duration of response)
ECOG: Eastern Co-operative Oncology Group
EV: Enfortumab Vedotin
HR: Hazard Ratio
ITT: Intent-to-treat
KI: Konfidenzintervall
ORR: Gesamtansprechrate (overall response rate)
OS: Gesamtüberleben (overall survival)
PD-L1: Programmierter Zelltod-Ligand 1 (programmed cell death ligand 1)
PFS: progressionsfreies Überleben (progression-free survival)
PR: partielles Ansprechen (partial response)
RECIST 1.1: Response Evaluation Criteria In Solid Tumors 1.1
TPS: tumor proportion score
UE: unerwünschtes Ereignis
ZNS: Zentralnervensystem
Quellen
- Powles T et al. Enfortumab Vedotin and Pembrolizumab in Untreated Advanced Urothelial Cancer. N Engl J Med 2024; 390(10):875–88 inkl. supplement.
- Fachinformation KEYTRUDA®, Stand August 2024.
DE-OBD-00117 08/24
Sie haben Fragen?
schnell – zuverlässig – kompetent
Unsere Ansprechpartner:innen
sind gerne für Sie da!
MSD Services
Vor der Verordnung eines Arzneimittels lesen Sie bitte die Fachinformation.
Fachinformationen
Gebrauchsinformationen
Sicherheitshinweise



