Biomarker
3 Tage – der Schlüssel zu mehr Perspektiven
Der Schlüssel zu mehr Perspektiven liegt in Ihrer Hand. Finden Sie jetzt heraus, wie Sie ihn einsetzen, um frühzeitig die bestgeeignete Therapieoption für Ihre Patienten zu finden.

Eine Testung von HNSCC-Tumoren auf eine PD-L1-Expression kann der Schlüssel sein, um bestimmten Patienten frühzeitig mehr Perspektiven in der Behandlung zu eröffnen. Einfach, schnell und kostengünstig können Sie wichtige Informationen erhalten, um eine möglicherweise lebensverlängernde Behandlungsentscheidung zu treffen.
Mehr Perspektiven für Ihre Patienten in nur 3 Tagen
KEYTRUDA® ist als Monotherapie zur neoadjuvanten Behandlung und anschließend zur adjuvanten Behandlung in Kombination mit Strahlentherapie mit oder ohne begleitende Cisplatin-Therapie und dann als Monotherapie des resezierbaren lokal fortgeschrittenen Plattenepithelkarzinoms der Kopf-Hals-Region bei Erwachsenen mit PD-L1-exprimierenden Tumoren (CPS ≥ 1) angezeigt.
Außerdem ist KEYTRUDA® als Monotherapie oder in Kombination mit Platin- und 5-Fluorouracil (5-FU)-Chemotherapie zur Erstlinienbehandlung des metastasierenden oder nicht resezierbaren rezidivierenden Plattenepithelkarzinom der Kopf-Hals-Region bei Erwachsenen mit PD-L1-exprimierenden Tumoren (CPS ≥ 1) angezeigt.
Therapie lokal fortgeschrittener Kopf-Hals-Tumore (PD-L1 CPS ≥ 1)
Perioperatives Behandlungsschema
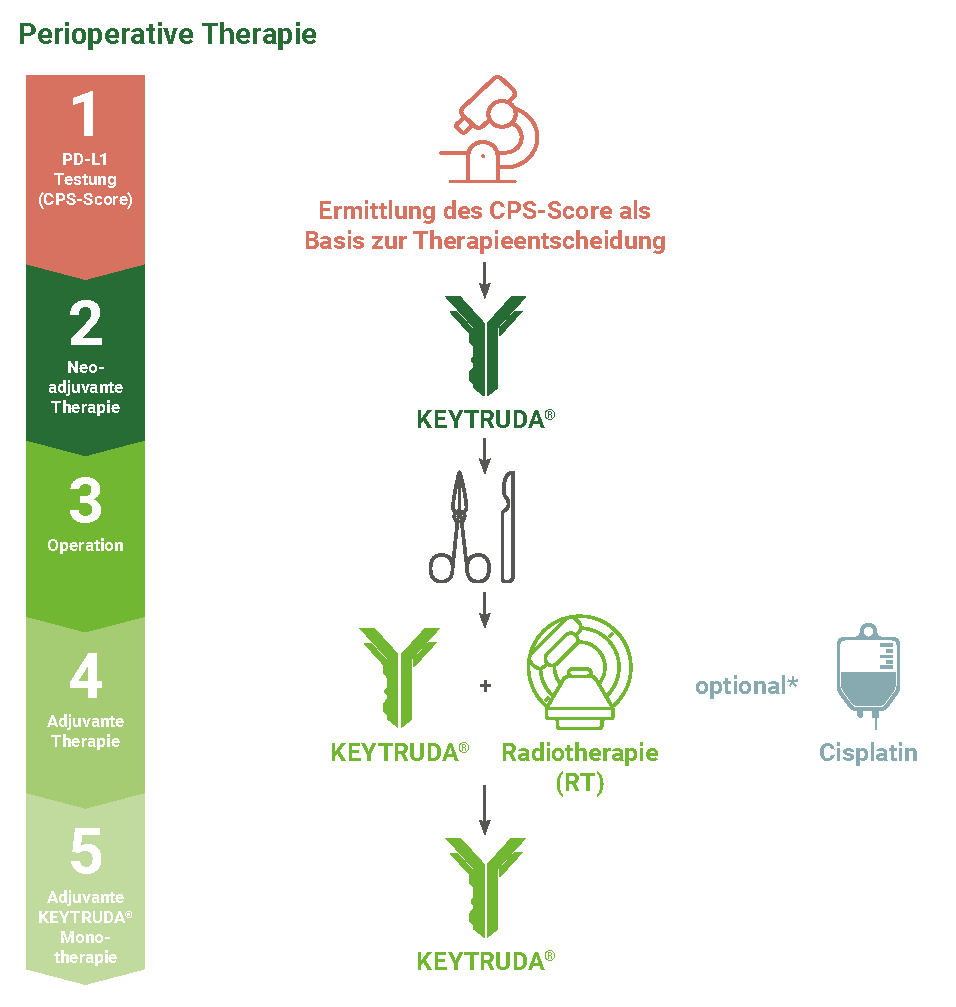
Abb. 1: Perioperatives HNSCC-Therapieschema: 1. PD-L1-Testung (CPS), 2. neoadjuvant KEYTRUDA®, 3. Operation, 4. adjuvant KEYTRUDA® + RT (± Cisplatin), 5. KEYTRUDA®-Monotherapie.1
Identifizieren Sie Ihre geeigneten Patienten frühzeitig für ein KEYTRUDA®-basiertes perioperatives Behandlungsregime mithilfe einer Testung auf PD-L1-Expression noch vor dem Tumorboard:1
- Die Testung kann der erste Schritt für eine personalisierte Therapie sein
- Die PD-L1-Testung ist einfach und kostengünstig
- Sie können mithilfe der Testung die Patienten finden, die am wahrscheinlichsten von einer Immuntherapie profitieren können
- Erfahren Sie jetzt mehr zur Relevanz der PD-L1-Testung bei Patienten mit fortgeschrittenen Kopf-Hals-Tumoren mit Prof. Dr. med. Sebastian Ochsenreither: Zum Video-Interview.
PD-L1 Testung – Individuell und bestmöglich therapieren. Testen Sie mit!
Ein Schlüssel zur Selektion geeigneter Patienten: Biomarker in der Präzisionsonkologie
In der Präzisionsonkologie dienen Biomarker als messbare Parameter und Indikatoren bei der molekulargenetischen und immunologischen Charakterisierung von Tumorerkrankungen.2 Diese molekulare, zelluläre und funktionelle Analyse des Tumors dient dazu, Krebspatienten eine möglichst individuelle und personalisierte Therapie anbieten zu können.3
Ein prädiktiver Biomarker wird verwendet, um Personen zu identifizieren, die mit höherer Wahrscheinlichkeit als Personen ohne diesen Biomarker von der Anwendung einer medizinischen Therapie profitieren oder im umgekehrten Fall nicht profitieren können.4
Einer dieser Biomarker ist der programmierte Zelltod-Ligand 1 (PD-L1), der im Tumorgewebe immunhistochemisch nachgewiesen werden kann. Exprimiert ein Tumor PD-L1 und wird diese Expression mithilfe einer Biomarker-Testung validiert, so kann bei bestimmten Tumoren eine Behandlung mit Immuncheckpoint-Inhibitoren in Frage kommen.5
Die Auswertung einer PD-L1-Färbung erfolgt nach spezifischen Auswertealgorithmen, sogenannten Scores. Diese unterscheiden sich darin, welche Zelltypen in die Bewertung mit einbezogen und wie diese zueinander ins Verhältnis gesetzt werden.5 Der relevante Score bei der Erstlinienbehandlung des M/uR HNSCC mit KEYTRUDA® sowie bei dem perioperativen Behandlungsregime im lokal fortgeschrittenen Stadium ist der Combined Positive Score (CPS).1
Testung auf PD-L1-Tumorexpression: CPS (Combined Positive Score)
Beim Combined Positive Score (CPS) handelt es sich um eine Bewertung PD-L1-positiv gefärbter Tumorzellen (partielle oder komplette Membranfärbung) und Immunzellen (Lymphozyten, Makrophagen) relativ zur Gesamtzahl vitaler Tumorzellen und multipliziert mit 100.6
![Formel zur Berechnung des CPS-Werts (Combined Positive Score) bei der PD-L1-Testung: CPS = (Anzahl PD-L1 positiver Zellen [Tumorzellen, Lymphozyten, Makrophagen] / Gesamtzahl vitaler Tumorzellen) × 100. Die Formel dient zur Einschätzung der Eignung für eine Immuntherapie basierend auf der PD-L1-Expression.](https://www.msdconnect.de/wp-content/uploads/sites/100/2025/04/CPS_9fa6b9.png?vip_files_acl=MTU3ODkwNDI1MXw0OTc2OQ%3D%3D)
Worauf ist bei der Übersendung von Tumormaterial an einen Pathologen zu achten?
- Verwenden Sie möglichst das neueste verfügbare Material5
- Eine formale Vorgabe, ob Primarius oder Metastase verwendet werden soll, gibt es bislang nicht5
- Sollte eine ausreichende Biopsie der aktuellen Metastase vorhanden sein, so ist diese zu bevorzugen5
- Das entnommene Tumormaterial muss mindestens 100 vitale Tumorzellen enthalten (bei KEYTRUDA®)5
Erfahren Sie mehr darüber, welche Informationen Pathologen benötigen, um die Gewebeprobe optimal zu beurteilen in unserem interaktiven Anforderungsformular.
Der pathologische Befund zur PD-L1-Expression ist die Grundlage, um Ihren geeigneten Patienten eine personalisierte Therapie mit KEYTRUDA® ermöglichen zu können.1
Kompakt zusammengefasst: Der prädiktive Wert des CPS beim HNSCC
In folgendem Video erfahren Sie, wie der CPS beim HNSCC genutzt werden kann und was er über die Wahrscheinlichkeit eines Therapieansprechens verrät:
Studie KEYNOTE-689: Neue Perspektiven durch perioperative Therapie beim LA HNSCC
Mit der Weiterentwicklung der Immuntherapie eröffnet sich auch im kurativen Setting des Kopf-Hals-Plattenepithelkarzinoms ein neuer Behandlungsansatz: KEYTRUDA® ist als Teil eines perioperativen Therapiekonzepts für erwachsene Patienten mit resezierbarem lokal fortgeschrittenem HNSCC und PD-L1-exprimierenden Tumoren (CPS ≥ 1) zugelassen.1, 7
Grundlage dieser Zulassung ist die Phase-III-Studie KEYNOTE-689, eine randomisierte, multizentrische, offene, aktiv kontrollierte Studie, die bei 714 Patienten mit resezierbarem lokal fortgeschrittenem (Stadium III oder IVA) HNSCC durchgeführt wurde. Haupteinschlusskriterien waren ein Alter ≥ 18 Jahre, eine histologisch bestätigte Neudiagnose eines resezierbaren, nicht metastasierten Plattenepithelkarzinoms sowie ein ECOG PS von 0 oder 1.1
Die Patienten erhielten entweder KEYTRUDA® als Teil eines perioperativen Regimes (neoadjuvant und adjuvant, jeweils vor und nach der OP) zusätzlich zu Resektion + adjuvanter Radiotherapie ± Cisplatin‡ (Studienarm A; n = 363; PD-L1 CPS ≥ 1 Population: n = 347), gefolgt von adjuvanter KEYTRUDA®-Monotherapie oder die aktuelle Standardtherapie bestehend aus Resektion + adjuvanter Radiotherapie ± Cisplatin‡ (Studienarm B; n = 351; PD-L1 CPS ≥ 1 Population: n = 335).1, 7 Studienarm A umfasste dabei eine neoadjuvante Phase mit KEYTRUDA® 200 mg i.v. alle 3 Wochen (2 Zyklen), gefolgt von Operation sowie eine adjuvante Phase mit KEYTRUDA® 200 mg i.v. Q3W (3 Zyklen) + Radiotherapie ± Cisplatin (100 mg/m² i.v., Q3W, 3 Zyklen), gefolgt von KEYTRUDA® 200 mg i.v. Q3W bis zu 12 Zyklen als Monotherapie, während Studienarm B aus Operation und adjuvanter Radiotherapie ± Cisplatin (100 mg/m² i.v., Q3W, 3 Zyklen) bestand.
Cisplatin (100 mg/m²) i.v. Q3W für 3 Zyklen wurde Patienten mit pathologischen Merkmalen für ein hohes Rezidivrisiko nach der Operation, definiert als positive Resektionsränder (< 1 mm im Primärresektat) oder extrakapsuläre Ausbreitung, verabreicht.
Der primäre Wirksamkeitsendpunkt war das ereignisfreie Überleben (EFS).
Die Ergebnisse unterstreichen, dass sich die Rolle der Biomarker-Testung weiterentwickelt: Sie kann nicht nur im metastasierten Setting, sondern auch entscheidend zur Therapieplanung im kurativen Setting beitragen.7, 8
Die Bestimmung der PD-L1-Expression mittels CPS gewinnt auch im lokal fortgeschrittenen HNSCC an Bedeutung: In der Studie KEYNOTE-689 waren weniger als 5 % der Patienten PD-L1-negativ (CPS < 1) oder ohne auswertbaren CPS.7
Retrospektive Studien zeigten, dass bei Populationen mit überwiegend Mundhöhlenkarzinomen eine PD-L1-Positivität von über 80 bis 90 % beobachtet wird.7
Dies unterstreicht die Relevanz der CPS-Bestimmung für die Identifikation geeigneter Patienten und die Therapieplanung.7
Erfahren Sie mehr zu den aktuellen Daten der Studie KEYNOTE-689.
S3-Leitlinie: KEYTRUDA® als Standard in der Erstlinientherapie
Die aktuelle S3-Leitlinie Diagnostik und Therapie des Mundhöhlenkarzinoms weist KEYTRUDA® in der Mono- oder Kombinationstherapie mit Platin- und 5-FU-Chemotherapie zur Erstlinienbehandlung des metastasierenden oder nicht resezierbaren rezidivierenden Plattenepithelkarzinoms der Kopf-Hals-Region (CPS ≥ 1) mit dem höchsten Empfehlungsgrad A aus.9
Der starke Empfehlungsgrad gilt für die Behandlung von Patienten mit PD-L1-exprimierenden Tumor- und Immunzellen (CPS ≥1) und bekräftigt den Stellenwert von KEYTRUDA® in der Erstlinientherapie (palliativ und palliativmedizinisch) bei Kopf-Hals-Tumoren (siehe Abb. 1).9
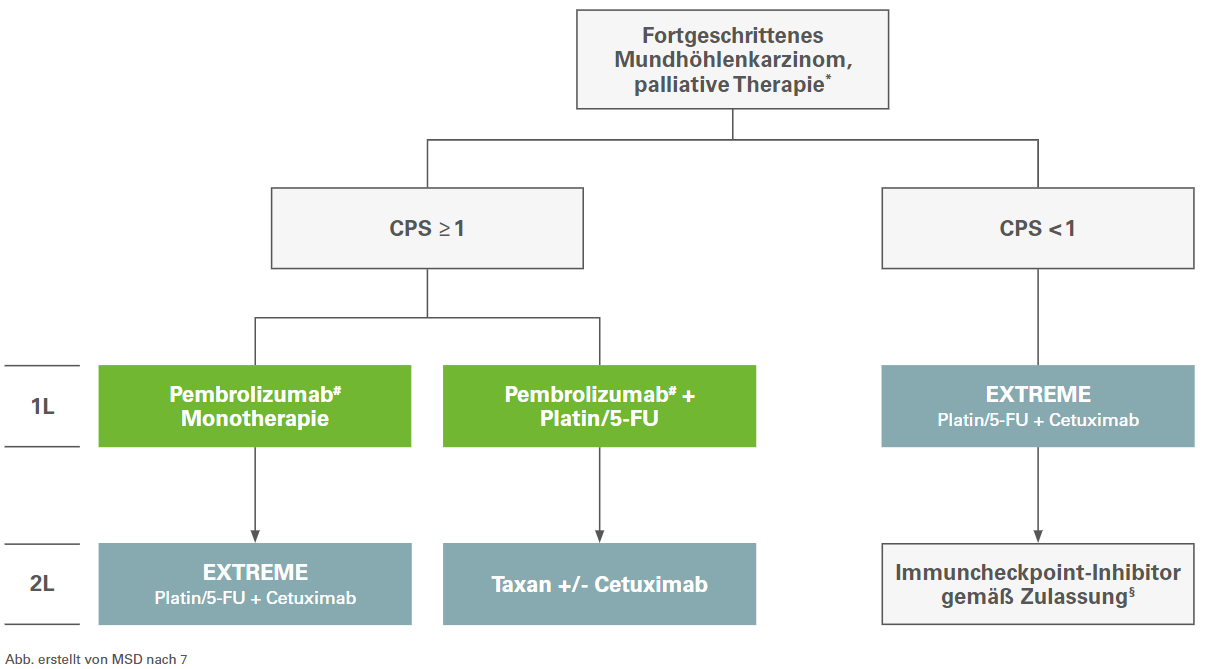
Abb. 1: Therapiealgorithmus nach Leitlinienempfehlung der aktuellen AWMF S3-Leitlinie für die palliative, systemische Behandlung des Mundhöhlenkarzinoms. Abbildung erstellt von MSD nach AWMF S3-Leitlinie Diagnostik und Therapie des Mundhöhlenkarzinoms.9
* nicht resezierbar, nicht operabel, keine kurative Option, rezidivierend oder Fernmetastasen.9
# KEYTRUDA® ist als Monotherapie oder in Kombination mit Platin- und 5-Fluorouracil (5-FU)-Chemotherapie zur Erstlinienbehandlung des metastasierenden oder nicht resezierbaren rezidivierenden Plattenepithelkarzinom der Kopf-Hals-Region bei Erwachsenen mit PD-L1-exprimierenden Tumoren (CPS ≥ 1) angezeigt.1
§ KEYTRUDA® ist zugelassen zur Behandlung des rezidivierenden oder metastasierenden HNSCC mit PD-L1-exprimierenden Tumoren (TPS ≥ 50 %) und einem Fortschreiten der Krebserkrankung während oder nach vorheriger Platin-basierter Therapie bei Erwachsenen.1
Erfahren Sie im Interview mit Prof. Dr. med. Andreas Dietz, Facharzt für Hals-Nasen-Ohren-Heilkunde, wie der Experte die Relevanz von S3-Leitlinien in der Onkologie sowie deren Empfehlung zur Diagnostik und Therapie des Mundhöhlenkarzinoms für den Therapiealltag einordnet.
KEYTRUDA® ist inzwischen in drei Leitlinien zur palliativen Erstlinienbehandlung bei PD-L1-positiven M/uR Kopf-Hals-Tumoren empfohlen und somit Therapie-Standard.9, 10, 8 Verschaffen Sie sich einen Überblick über eine leitliniengerechte Therapie.
Onkopedia-Leitlinie Kopf-Hals-Plattenepithelkarzinom
Lesen Sie das Interview mit dem Erstautor der Onkopedia-Leitlinie zur Diagnostik und Therapie des Kopf-Hals-Plattenepithelkarzinoms. Werfen Sie einen Blick hinter die Kulissen: Im Interview gibt PD Dr. Konrad Klinghammer einen Einblick in die Entstehung und Bedeutung der Onkopedia-Leitlinien. Jetzt mehr dazu erfahren.
KEYNOTE-048: Eine Studie, die die Relevanz der PD-L1-Testung unterstreicht
Die Studie KEYNOTE-048 ist eine multizentrische, offene, randomisierte und aktiv kontrollierte Phase-3-Studie bei Patienten mit histologisch bestätigtem metastasierenden oder nicht resezierbaren rezidivierenden HNSCC ohne systemische Vorbehandlung und die als nicht heilbar durch lokale Therapien galten.10
Unter den 882 Patienten in der Studie KEYNOTE-048 waren 754 Patienten (85 %), deren Tumore PD-L1 mit einem CPS ≥ 1 exprimierten und 381 (43 %) mit einem CPS ≥ 20.10
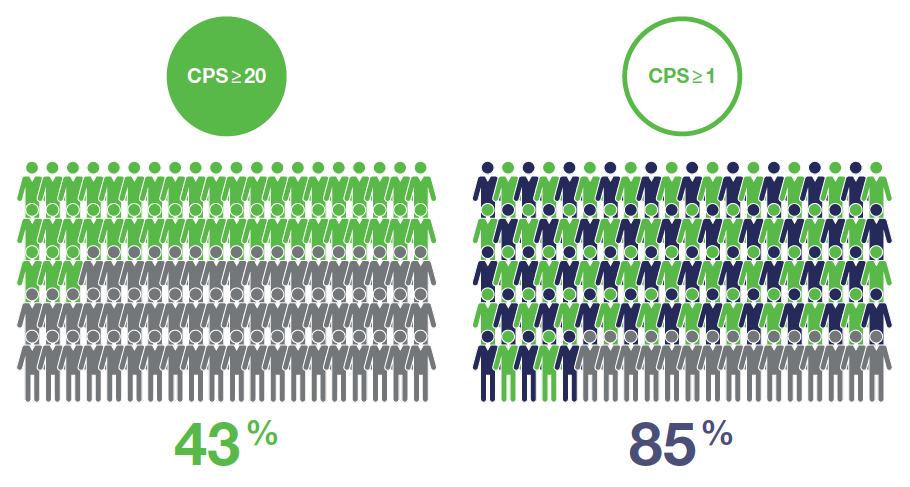
Abb. 2: Prozentualer Anteil der Patienten der Studie KEYNOTE-048, deren Tumore PD-L1 mit einem CPS ≥ 1 (85 %) und einem CPS ≥ 20 (43 %) exprimierten. Grafik erstellt von MSD nach Daten von Burtness et al., 2019.10
85 % der Studienteilnehmer in der Studie KEYNOTE-048 hatten einen PD-L1 CPS ≥ 1 (s. Abb. 2).10 Die ausführlichen Ergebnisse der Studie KEYNOTE-048 finden Sie in einer kompakten Übersicht in unserer Abgabekarte.
Identifizieren Sie Ihre geeigneten Patienten und eröffnen Sie die Chance auf Langzeitüberleben
Studie KEYNOTE-048: 5-Jahres-Langzeitdaten
Für die Erstlinientherapie des M/uR HNSCC (PD-L1 CPS ≥ 1) gibt es klinisch relevante Langzeitdaten der Studie KEYNOTE-048 .11 Mit einer Nachbeobachtungszeit von 5 Jahren hat sie die bislang längste Nachbeobachtungszeit für eine Anti-PD-1-Therapie beim fortgeschrittenen HNSCC in der Erstlinientherapie.11
Erfahren Sie mehr zu den aktualisierten 5-Jahres-Daten der Studie KEYNOTE-048.
Interaktive Fallpräsentation: Erleben Sie einen echten HNSCC-Patientenfall virtuell

Mit unseren interaktiven eKasuistiken haben Sie nun die Möglichkeit, Ihr Wissen anhand von echten Patientenfällen anzuwenden und zu testen.
Lernen Sie jetzt unterschiedliche Therapieansätze kennen, finden Sie heraus, wie Ihre Kollegen therapiert hätten und erkennen Sie die Bedeutung der PD-L1-Testung im Zusammenhang mit echten Patientenfällen: Zu den Kasuistiken
Bedenken Sie eine frühe, biomarkerbasierte Therapieentscheidung über verschiedene Krankheitsstadien hinweg!
Anmerkungen
‡ Strahlentherapie ± Cisplatin (100 mg/m2) i.v. Q3W (3 Zyklen).
± Das ereignisfreie Überleben mittels BICR gemäß RECIST v.1.1 war definiert als die Zeit von der Randomisierung bis zum radiologischen Progress der Erkrankung während der neoadjuvanten Phase, der eine Operation verhindert, bis zum lokalen oder distanten Progress/Rezidiv in der Bildgebung oder Biopsie oder bis zum Tod aus jeglicher Ursache.
£ Basierend auf dem Cox-Regressionsmodell mit Efron-„Tie-Handling“- Methode, wobei die Behandlung als Kovariate stratifiziert wurde nach primärer Tumorlokalisation und Tumorstadium.$ Das Protokoll sah die Angabe einseitiger p-Werte vor; einseitiger p-Wert basierend auf dem Log-Rank-Test, stratifiziert nach primärer Tumorlokalisation und Tumorstadium. Im Vergleich zum einseitigen p-Wert-Grenzwert von 0,0124 in der CPS ≥ 1-Population; gemäß den Richtlinien der Publikation werden zweiseitige p-Werte angegeben.
Abkürzungen
5-FU: 5-Fluorouracil
CPS: Combined Positive Score
ESMO: European Society for Medical Oncology
HNSCC: Plattenepithelkarzinom der Kopf-Hals-Region (head and neck squamous cell carcinoma)
M/uR: Metastasierend oder nicht resezierbar rezidivierend
PD-L1: Programmierter Zelltod-Ligand 1 (programmed cell death ligand 1)
TPS: Tumor Proportion Score
Quellen
- Fachinformation KEYTRUDA®.
- Reininghaus S, Oettler D. Biomarker in der Präzisionsonkologie – Stellenwert in der personalisierten Versorgung von Krebserkrankungen, Seite 198–219: Beitrag in: Gesundheitswesen aktuell 2021: BARMER Institut für Gesundheitsforschung (bifg) [cited 20.03.26]. Available from: URL: https://www.barmer.de/resource/blob/1031944/11b7bb6292899480a7defa62f0e4525c/bifg-gw-aktuell-2021-biomarker-in-der-praezisionsonkologie-data.pdf.
- NCT (Nationales Centrum für Tumorerkrankungen Heidelberg). Präzisionsonkologie [cited 20.03.26]. Available from: URL: www.nct-heidelberg.de/das-nct/kernbereiche/translationale-medizinische-onkologie/schwerpunkte/praezisionsonkologie.html.
- FDA-NIH Biomarker Working Group. BEST (Biomarkers, EndpointS, and other Tools) Resource: Predictive Biomarker. Silver Spring (MD): Food and Drug Administration (US); 2016 [cited 20.03.26]. Available from: URL: https://www.ncbi.nlm.nih.gov/books/NBK402283/.
- Schildhaus H-U. Der prädiktive Wert der PD-L1-Diagnostik. Pathologe 2018; 39(6):498–519.
- Agilent Technologies. PD-L1 IHC 22C3 pharmDx Interpretation Manual – Head and Neck Squamous Cell Carcinoma (HNSCC): FDA-approved for in vitro diagnostic use [Rx only]; 2023 [cited 20.03.26].
- Uppaluri R et al. Neoadjuvant and Adjuvant Pembrolizumab in Locally Advanced Head and Neck Cancer. N Engl J Med 2025; 393(1):37–50.
- DGHO. Onkopedia Leitlinien. Kopf-Hals-Plattenepithelkarzinome: Stand: Oktober 2022 [cited 2026 Mar 17]. Available from: URL: https://www.onkopedia.com/de/onkopedia/guidelines/kopf-hals-plattenepithelkarzinome/@@guideline/html/index.html.
- Deutsche Krebsgesellschaft, Deutsche Krebshilfe, AWMF (Leitlinienprogramm Onkologie). S3 Leitlinie Diagnostik und Therapie des Mundhöhlenkarzinoms. Langversion 3.0 – März 2021 [AWMF-Registernummer: 007/100OL] [cited 20.03.26]. Available from: URL: https://www.leitlinienprogramm-onkologie.de/fileadmin/user_upload/Downloads/Leitlinien/Mundhoehlenkarzinom/Version_3/LL_Mundhoehlenkarzinom_Langversion_3.0.pdf.
- Leitlinienprogramm Onkologie [Deutsche Krebsgesellschaft, Deutsche Krebshilfe, AWMF]. S3-Leitlinie Diagnostik, Therapie, Prävention und Nachsorge des Oro- und Hypopharynxkarzinoms: Version 1.0 – März 2024 [AWMF-Registernummer: 017-082OL]; 2026. Available from: URL: https://www.leitlinienprogramm-onkologie.de/fileadmin/user_upload/Downloads/Leitlinien/Oro-_und_Hypopharynxkarzinom/LL_Oro-_und_Hypopharynxkarzinom_Langversion_1.0.pdf.
- Tahara M et al. Pembrolizumab with or without chemotherapy in recurrent or metastatic head and neck squamous cell carcinoma: 5-year follow-up from the randomized phase III KEYNOTE-048 study. Eur J Cancer 2025; 221:115395.
DE-OHN-00291 05/26
Sie haben Fragen?
schnell – zuverlässig – kompetent
Unsere Ansprechpartner:innen
sind gerne für Sie da!
MSD Services
Vor der Verordnung eines Arzneimittels lesen Sie bitte die Fachinformation.
Fachinformationen
Gebrauchsinformationen
Sicherheitshinweise



